单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点越高。下列溶液中沸点最高的是
| A.0.01 mol/L的蔗糖溶液 | B.0.01 mol/L的K2SO4溶液 |
| C.0.02 mol/L的NaCl溶液 | D.0.02 mol/L的CH3COOH溶液 |
长式周期表共有18个纵行,从左到右排为1—18列,即碱金属为第一列,稀有气体元素为第18列。按这种规定,下列说法正确的是 ()
| A.s区元素都是金属元素 | B.第13列的元素原子最外层电子排布为ns2 np1 |
| C.第四周期第9列元素是铁元素 | D.第10、11列为ds区 |
下列化学用语说法正确的是( )
A.过氧化钠的电子式: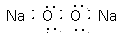 |
B.钾元素的原子结构示意图为:K  |
| C.次氯酸的结构式: H-O-Cl |
D.硫原子的电子排布图为: |
1s 2s 2p 3s 3p
下列说法中正确的是()
①CO2与CS2互为等电子体;
②同一周期从左到右,元素的电负性、原子的半径都是越来越大;
③价电子数等于族序数;
④含有阳离子的晶体一定是离子晶体;
⑤温度越高,金属的导电性越好;
⑥熔融状态下能导电的化合物一定是离子晶体;
⑦P4和CH4都是正四面体分子且键角都为109o28ˊ。
| A.①②③ | B.⑤⑥⑦ | C.①④⑥⑦ | D.①⑥ |
硼和镁形成的化合物刷新了金属化合物超导温度的最高记录。如图是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下面还各有一个镁原子;6个硼原子位于棱柱的侧棱上,则该化合物的化学式可表示为()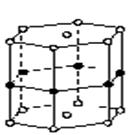
| A.MgB | B.Mg3B2 | C.MgB2 | D.Mg2B3 |
在通常条件下,下列各组物质的性质排列正确的是()
| A.熔点:HF>HCl>HBr | B.水溶性:HCl>CO2>SO2 |
C.沸点: 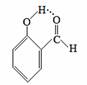 > >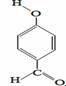 |
D.热稳定性:HCl>H2S>PH3 |