用一种阴、阳离子双隔膜三室电解槽处理废水中的NH4+,模拟装置如图所示。下列说法正确的是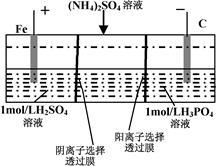
| A.阳极室溶液由无色变成棕黄色 |
| B.阴极的电极反应式为:4OH–-4e–=2H2O+O2↑ |
| C.电解一段时间后,阴极室溶液中的pH升高 |
| D.电解一段时间后,阴极室溶液中的溶质一定是(NH4)3 PO4 |
元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是( )
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.P,S,Cl得电子能力和最高价氧化物对应水化物的酸性均依次增 |
| D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
金属加工后的废切削液中含2—5%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理此废切削液,使NaNO2转化为无毒物质。该反应分两步进行:
第一步:NaNO2+NH4Cl=NaCl+NH4NO2第二步:NH4NO2= N2↑+2H2O
下列对第二步反应的叙述中正确的是( )
①NH4NO2是氧化剂② NH4NO2是还原剂③ NH4NO2发生了分解反应
④只有氮元素的化合价发生了变化⑤ NH4NO2既是氧化剂又是还原剂
| A.①③ | B.①④ | C.②③④ | D.③④⑤ |
下列离子方程式书写正确的是 ( )
A. NaHS水解:HS-+H2O="==" H3O++S2-
B、、KOH溶液吸收过量SO2:OH-+SO2===HSO3-
C向氯化铁溶液中加入少量氨水制氢氧化铁胶体:3NH3•H2O+Fe3+===3NH4++Fe(OH)3(胶体)
D、向BaCl2溶液中通入少量CO2气体:Ba2++CO2+H2O===BaCO3↓+2H+
下列离子组能大量共存的是( )。
| A.使甲基橙呈黄色的溶液中:I-、Cl-、NO3-、Na+ |
| B.使石蕊呈蓝色的溶液中:Na+、AlO2-、NO3-、HCO3- |
| C.加入铝粉能产生氢气的溶液中,可能存在大量的Na+、Ba2+、AlO2-、NO3- |
| D.含大量Fe3+的溶液中:K+、NH4+、SO42-、SCN- |
设NA为阿伏加德罗常数的值,下列叙述正确的是 ( )
| A.标准状况下, 22.4 L CH2Cl2含有分子数为NA |
| B.分子总数为NA的N2、C2H4混合气体体积约为22.4 L,质量为28 g |
| C.常温常压下,1mol 丙烯分子中含共价键数为6NA |
| D.足量的CO2与39 g Na2O2发生反应,转移的电子数为0.5NA |