已知2H2O2  2H2O+ O2↑,若其他条件不变,下列措施不能使该反应速率增大的是( )
2H2O+ O2↑,若其他条件不变,下列措施不能使该反应速率增大的是( )
| A.降低温度 |
| B.加入少量MnO2 |
| C.加入少量FeCl3 |
D.增大H2O2的浓度 |
将等物质的量的金属Na、Mg、Al分别与100 mL 2 mol·L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法错误的是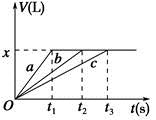
| A.x=2.24 |
| B.钠的物质的量为0.2 mol |
| C.反应时,Na、Mg、Al均过量 |
| D.曲线b为Mg与盐酸反应的图像 |
海水是重要的资源。可以制备一系列物质
下列说法正确的是
| A.步骤②中,应先通CO2,再通NH3 |
| B.步骤③可将MgCl2·6H2O晶体在空气中直接加热脱水 |
| C.步骤④、⑤、⑥反应中,溴元素均被氧化 |
D.除去粗盐中的 、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸 、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸 |
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下: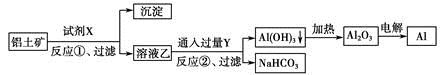
下列叙述正确的是
| A.试剂X可以是氢氧化钠溶液,也可以是盐酸 |
| B.反应①、过滤后所得沉淀为氢氧化铁 |
| C.图中所示转化反应都不是氧化还原反应 |
| D.反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3 |
下列反应的离子方程式正确的是
| A.稀硫酸与铁反应:2Fe+6H+=2Fe3++3H2↑ |
| B.2 mol·L-1的AlCl3溶液和7 mol·L-1的NaOH溶液等体积均匀混合: 2Al3++7OH-=Al(OH)3↓+ 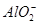 +2H2O +2H2O |
| C.Ba(OH)2溶液中加入少量的NaHSO4溶液: Ba2++2OH-+2H++  =BaSO4↓+2H2O =BaSO4↓+2H2O |
D.NaHCO3的水解: +H2O +H2O  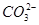 +H3O+ +H3O+ |
在1 L含0.1 mol NaAlO2和0.1 mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.1 mol·L-1H2SO4溶液,下列图像中能表示反应产生沉淀的物质的量与加入硫酸溶液体积之间关系的是