[化学—化学与技术]
硫酸是一种重要的化工原料,硫酸工业的“三废”处理之一是对尾气处理,其中一种方法便是用天然海水进行尾气脱硫。
(1)硫酸工业生产的主要设备有 、 和吸收塔。在吸收塔内装有大量磁环的作用是 ,浓硫酸从塔顶喷下,SO3吸收操作采取 形式(原理);硫酸工业的尾气主要成分有SO2、O2、N2等。
(2)天然海水主要含有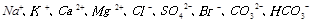 等离子。
等离子。
①天然海水pH约为8,原因是海水中 离子水解所致。
②尾气进入吸收塔内,塔顶喷下大量海水,O2能将 、
、 、
、 等氧化,试写出其中一个反应的方程式: 。
等氧化,试写出其中一个反应的方程式: 。
③向氧化后的海水中加入天然海水,其目的是中和、稀释氧化后海水中生成的酸,最终排放出的海水中 浓度与进入吸收塔的天然海水相比,
浓度与进入吸收塔的天然海水相比, 浓度 (填序号)。
浓度 (填序号)。
| A.减少 | B.增大 | C.不变 | D.无法判断 |
将5.3 g某碱式碳酸盐固体(不含结晶水)M溶解于100 g 9.8%的稀硫酸中,充分反应后得到 224 mL CO2(标准状况)和含有MgSO4、Al2(SO4)3的溶液。向所得溶液中逐滴加入NaOH溶液,产生沉淀的质量与加入的溶质NaOH的质量关系如图所示。
(1)由图可知,固体M与稀硫酸反应后所得溶液中除含有溶质MgSO4和Al2 (SO4)3外,还含有的溶质是 (写化学式)。
(2)加入的溶质NaOH从x g到8.8 g所发生反应的离子方程式为 。
(3)当加入溶质NaOH的质量到xg时,生成Al(OH)3的质量为 g,x= 。
(4)M的化学式为 。
铁是目前人类使用量最大的金属,它能形成多种化合物。
(1)取5.6 g的生铁与足量的稀硫酸混合反应,无论怎样进行实验,最终收集了的气体体积均小于2.24 L(标准状况),最主要的原因是__________,所得溶液在长时间放置过程中会慢慢出现浅黄色,试用离子方程式解释这一变化的原因____________。
(2)ZnFe2Ox是一种新型纳米材料,可将工业废气中的某些元素转化为游离态,制取纳米ZnFe2Ox 和用于除去废气的转化关系如图 。若上述转化反应中消耗的
。若上述转化反应中消耗的 ,x的值为_________________。请写出 ZnFe2Ox与NO2反应的化学方程式______________(x用前一问求出的具体值)。
,x的值为_________________。请写出 ZnFe2Ox与NO2反应的化学方程式______________(x用前一问求出的具体值)。
(3)LiFePO4(难溶干水)材料被视为最有前途的锂离子电池材料之一。
①以 FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4 ,,该反应还生成一种可燃性气体,则反应方程式为____________.
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负桩隔开)工作原理为 。则放电时正极上的电极反应式为___________.
。则放电时正极上的电极反应式为___________.
(4)已知25℃时,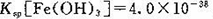 ,此温度下若在实验室中配制5 mol/L 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加人2 mol/L的盐酸__________ml(忽略加入盐酸体积)。
,此温度下若在实验室中配制5 mol/L 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加人2 mol/L的盐酸__________ml(忽略加入盐酸体积)。
有A、B、C、D、E、F六种元素。已知:
①它们位于三个不同的短周期,核电荷数依次增大。
②B与F同主族。
③B、C分别都能与D按原子个数比1∶1或1∶2形成化合物。
④A、E分别都能与D按原子个数比1∶1或2∶1形成化合物。
⑤E元素的电离能数据如下 (kJ·mol-1):
| I1 |
I2 |
I3 |
I4 |
… |
| 496 |
4562 |
6912 |
9540 |
… |
(1)写出只含有A、B、D、E四种元素的两种无水盐的化学式________、________。
(2)B2A4分子中存在______个σ键,______个π键。
(3)人们通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于计算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
| 化学键 |
A—A |
C—C |
A—C |
| 键能/kJ·mol-1 |
436 |
946 |
390.8 |
试计算A单质与C单质反应生成CA3时的反应热ΔH=_____ (要写单位)。
(8分) Q、R、X、Y、Z五种元素的原子序数依次递增。已知:①Z的原子序数为29,其余的均为短周期主族元素;②Y原子价电子(外围电子)排布为msnmpn;③R原子核外L层电子数为奇数;④Q、X原子p轨道的电子数分别为2和4。请回答下列问题:
(1)Z2+的核外电子排布式是_____________。
(2)在[Z(NH3)4]2+离子中,Z2+的空轨道接受NH3分子提供的______形成配位键。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是__________。
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小至大的顺序为___________ (用元素符号作答)。
(5)Q的一种氢化物相对分子质量为26,其分子中σ键与π键的键数之比为______。
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于______(填晶体类型)。
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B二种元素组成的原子个数比为1:1的化合物N是常见的有机溶剂。E的原子序数为26。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)下列叙述正确的是___________。(填字母)
a.M分子空间构型为平面三角形,而BD2为直线形,BA4为正四面体形
b.M和BD2分子中的中心原子均采取sp2杂化,而CA3分子中采取sp3杂化
c.N 是非极性分子,且分子中σ键 和π键的个数比为3:1
d.BD2晶体的熔点、沸点都比二氧化硅晶体的低
(2)B、C、D三种元素的电负性由小到大的顺序为_______;C的第一电离能大于D的第一电离能原因是_______。
(3)化合物CA3的沸点比化合物BA4的高,其主要原因是_________。
(4)B、D、E三元素能形成化合物E(BD)5,常温下呈液态,熔点为-20.5℃,沸点为103℃。据此可判断E(BD)5晶体为__________。基态E2+离子的电子排布式为_________。
(5)化合物BD与元素B、C形成的阴离子互为等电子体,阴离子的化学式是_________。