模拟侯氏制碱法原理,在CaCl2浓溶液中通入NH3和CO2可制得纳米级材料,装置见下图。下列说法正确的是( )
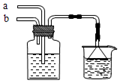
| A.a通入适量的CO2,b通入足量的NH3,纳米材料为Ca(HCO3)2 |
| B.a通入足量的NH3,b通入适量的CO2,纳米材料为Ca(HCO3)2 |
| C.a通入适量的CO2,b通入足量的NH3,纳米材料为CaCO3 |
| D.a通入少量的NH3,b通入足量的CO2,纳米材料为CaCO3 |
下列化学实验事实及其结论都正确的是( )
| 选项 |
实验事实 |
结论 |
| A |
将SO2通入含HClO的溶液中生成H2SO4 |
HClO酸性比H2SO4强 |
| B |
铝箔在酒精灯火焰上加热熔化但不滴落 |
铝箔表面氧化铝熔点高于铝 |
| C |
SiO2可以和NaOH溶液及HF溶液反应 |
SiO2属于两性氧化物 |
| D |
将SO2通入溴水中,溴水褪色 |
SO2具有漂白性 |
用黄色的FeCl3溶液分别进行下列实验,解释或结论不正确的是( )
| 选项 |
实验 |
现象 |
解释或结论 |
| A |
加入FeCl3固体 |
溶液变成红褐色 |
FeCl3的水解程度变大 |
| B |
加入等体积水 |
溶液颜色变浅 |
c(Fe3+)变小 |
| C |
加入足量Fe粉 |
溶液颜色变成浅绿色 |
2Fe3++Fe=3Fe2+ |
| D |
将FeCl3溶液微热 |
溶液变成红褐色 |
水解反应 ΔH>0 |
下表中各组物质不能实现如图转化的是( )
| 选项 |
甲 |
乙 |
丙 |
| A |
AlCl3 |
Al |
Al(OH)3 |
| B |
AlCl3 |
Al(OH)3 |
NaAlO2 |
| C |
CO2 |
NaHCO3 |
Na2CO3 |
| D |
CO2 |
(NH4)2CO3 |
NH3 |
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
| A.甲醇 | B.天然气 | C.液化石油气 | D.氢气 |
下列关于常见有机物的说法不正确的是( )
| A.淀粉、蛋白质、油脂都属于天然高分子化合物 |
| B.糖类和蛋白质都是人体重要的营养物质 |
| C.乙烯和甲烷可用酸性高锰酸钾溶液鉴别 |
| D.乙酸和油脂都能与氢氧化钠溶液反应 |