根据原电池的知识回答下列问题。
(1)下图烧杯中溶液为稀硫酸,则观察到Al上的现象是 。
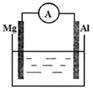
(2)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如下图所示:A、B两个电极均由多孔的碳块组成。该电池的正极反应为: 。

(3)如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电池装置,电池的总反应方程式为:CH4+2O2+2KOH=K2CO3+3H2O,则该电池的负极反应式为 。
(4)铅蓄电池放电时反应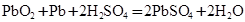 ,若放电消耗2mol硫酸时电路中转移电子_________mol
,若放电消耗2mol硫酸时电路中转移电子_________mol
维生素C是一种水溶性维生素(其水溶液呈酸性),它的化学式是C6H8O6,人体缺乏这样的维生素能得坏血症,所以维生素C又称抗坏血酸。在新鲜的水果、蔬菜、乳制品中都富含维生素C,例如新鲜橙汁中维生素C的含量在500mg/L左右。十二中某研究性学习小组测定了某品牌软包装橙汁中维生素C的含量,下面是他们的实验分析报告。
(一)测定目的:测定×××牌软包装橙汁中维生素C的含量。
(二)测定原理:C6H8O6+I2 →C6H6O6+2H++2I―
(三)实验用品及试剂
(1)仪器和用品(自选,略)
(2)试剂:指示剂_________(填名称,1分),浓度为8.00×10-3mol·L-1的I2标准溶液、蒸馏水等。
(四)实验过程
(3)洗涤仪器,检查滴定管是否漏液,润洗相关仪器后,装好标准碘溶液待用。
(4)用________________(填仪器名称,1分)向锥形瓶中移入20.00mL待测橙汁,滴入2滴指示剂。
(5)用左手控制滴定管的____________(填部位,1分),右手摇动锥形瓶,眼睛注视___________,直到滴定终点。滴定至终点时的现象是________________。
(五)数据记录与处理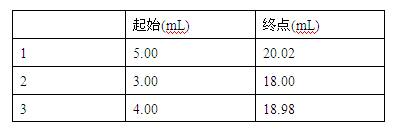
(6)若经数据处理,则此橙汁中维生素C的含量是____________mg/L。
(六)问题讨论
(7)从分析数据看,此软包装橙汁是否是纯天然橙汁?_______(填“是”或“不是”或“可能是”,1分)。生产商最可能采取的做法是__________(填编号,1分):
A.加水稀释天然橙汁 B.将维生素C作为添加剂 C.橙汁已被浓缩
实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成,取mg该种氨基酸放在纯氧中充分燃烧。生成CO2、H2O和N2。现按下图装置进行实验,请完成下列问题: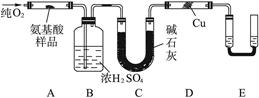
(1)实验开始时,首先要通入一段时间的氧气,其理由是__________________________。
(2)以上装置中需要加热的仪器有________(填字母),操作时应先点燃______处的酒精灯。
(3)A装置中发生反应的化学方程式为____________________________________。
(4)装置D的作用是_______________________________。
(5)读取N2的体积时,应注意①__________________,②___________________________。
(6)实验中测得N2的体积为VmL(已折算成标准状况),为确定此氨基酸的分子式,还需要的有关数据有__________。
| A.生成CO2气体的质量 |
| B.生成水的质量 |
| C.通入O2的体积 |
| D.氨基酸的相对分子质量 |
长期存放的亚硫酸钠可能会被部分氧化,现通过实验来测定某无水亚硫酸钠试剂的纯度。实验步骤如下:
①称量a g样品,置于烧杯中。
②加入适量蒸馏水,使样品溶解。
③加入稀盐酸,使溶液呈强酸性,再加过量的BaCl2溶液。
④过滤,用蒸馏水洗涤沉淀。
⑤加热干燥沉淀物。
⑥将沉淀物冷却至室温后,称量。
⑦重复⑤⑥操作直到合格,最后得到b g固体。
完成下面问题:
(1)本实验中是否能用Ba(NO3)2代替BaCl2?(填“能”或“不能”)其理由是:
________________________________________________________________________。
(2)步骤③中加盐酸,使溶液呈强酸性的目的是:
____________________________________________________________________________。
(3)步骤⑦的“合格”标准是:__________________________________________________。
(4)实验测得的样品中无水亚硫酸钠的质量分数是:__________(列出算式,不需要化简)。
(Ⅰ)用质量分数为98%的浓硫酸(密度为1.84g/cm3)配制成1mol/L的稀硫酸.现实验室仅需要这种硫酸220mL.试回答下列问题:
(1)配制稀硫酸时,应选用容量为________mL的容量瓶;
(2)经计算需要用量筒量取_______mL浓硫酸,在量取时宜选用下列量筒中的____(填字母).
| A.5mL | B.10mL | C.25mL | D.50mL |
(3)在量取浓硫酸后,进行了下列操作:
①等稀释的硫酸其温度与室温一致后,沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水至液面接近环形标线1-2cm处,改用胶头滴管加蒸馏水,使溶液的凹液面底部与瓶颈的环形标线相切。
③将浓硫酸缓缓注入盛适量蒸馏水的烧杯中,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)________________。
(4)容量瓶使用之前,检查其是否漏水的具体操作为
。
(5)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓硫酸,其配制的稀硫酸浓度会________(填“偏高”、“偏低”、“无影响”)。
(Ⅱ)某同学称量mgNaOH固体配制V m L 4mol/L的NaOH溶液,下面是该同学配制过程的示意图,其操作中错误的是(填操作序号)。
某中学化学实验小组为了证明和比较SO2与氯水的漂白性,设计了如下装置:
(1)实验室常用装置E制备Cl2,指出该反应中浓盐酸所表现出的性质______、_______。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管加热,两个试管中的现象分别为:
B ,
D。
(3)装置C的作用是。
(4)该实验小组的甲、乙两位同学利用上述两发生装置按下图装置继续进行实验:
通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅。试根据该实验装置和两名同学的实验结果回答问题。
①试分析甲同学实验过程中,品红溶液不褪色的原因是
,
反应的离子方程式是;
②你认为乙同学是怎样做到让品红溶液变得越来越浅的?
。