铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)。
(1)硝酸在该反应中的作用是__________________。该反应的还原产物是________________
(2)0.4molCu被硝酸完全溶解后,硝酸得到的电子数是______________,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是______________。
(1)以基态硅原子为例,如果电子排布式写作ls22s22p63s13p3则违反了原理,如写作ls22s22p63s33p1则违反了原理;
(2)已知H、C、Si三种元素的电负性依次为2.1、2.5、1.8,则CH4、SiH4中C、Si的化合价依次为、;
(3)在我们现今使用的元素周期表中,元素种类最多的族是族,共种元素;元素种类最多的周期是第周期,共种元素;
(4)熔点: F2Cl2(填“<”或“=”“或>”,下同),沸点:HFHCl,一定压强下HF和HCl的混合气体降温时(填HF或HCl)先液化;
(5)前三周期元素中,基态原子中未成对电子数与其所在周期序数相同的元素:
(用元素符号按原子序数由小到大排列)。
室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下面的框图进行反应。又知E溶液是无色的。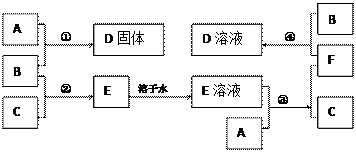
请回答:
(1)写出A、B、C的化学式。
A:B:C:
(2)反应①的化学方程式为:
(3)反应③的化学方程式为:
(4)反应④的离子方程式为:
某可逆反应从0—2分钟进行过程中,在不同反应时间各物质的量的变化情况如图
所示。
⑴则该反应的的反应物,生成物是,化学方程式为;
⑵能否计算反应开始至2分钟时,用C表示的反应速率?若能,其反应速率为,
若不能,则其原因为 __;
⑶2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了_________状态。
(9分) W.X.Y.Z是原子序数依次增大的同一短同期元素,W.X是金属元素,Y.Z是非金属元素。
(1)W.X各自的最高价氧化物对应的水化物可以反应生盐和水,该反应的离子方程式为________________。
(2)W与Y 可形成化合物W2Y,该化合物为 (填离子化合物或共价化合物)
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的离子方程式为___________。
(4)比较Y.Z气态氢化物的稳定性>(用化学式表示)
(5)W.X.Y.Z四种元素简单离子的离子半径由大到小的顺序是:
>>>。(用化学式表示)
(6)Z的最高价氧化物为无色液体,该物质与一定量水混合得到一种稀溶液,试写出该反应的化学方程式:_______________________。
现有如下两个反应:(A)NaOH + HCl =" NaCl" + H2O
(B)2FeCl3 + Cu = 2FeCl2 + CuCl2
(1)根据两反应本质,判断能否设计成原电池A:, B:______(填“能”与“不能”)
如果不能,说明其原因
(2)根据能设计成原电池的反应选择适宜的材料和试剂设计一个原电池:
①负极材料是, 正极材料是_______,电解质溶液是;
②写出正极的电极反应式,正极发生反应(填“氧化”或“还原”),
③若导线上转移电子0.1mol,则负极质量变化克。