化学与人类生活密切相关。请按要求,回答下列问题:
(1)漂白粉有效成分的化学式为 ,其能消毒杀菌是因有强 性。
(2)KAl(SO4)2•12H2O的俗名为 ,因其溶于水生成 而具有净水作用。
(3)酸雨的pH小于 ,含亚硫酸的酸雨久置后pH (增大、减小或不变)。
(4)小苏打可用于治疗胃酸过多,其反应的离子方程式为 。
(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
________+________→________+________+________+H2O
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1mol氧化剂_______(填“得到”或“失去”)________mol电子。
下图是煤化工产业链的一部分,试运用所学知识,解决下列问题: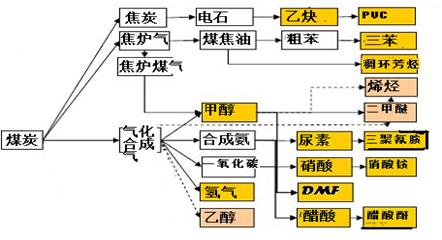
(1)该产业链中合成氨的反应在较低温下能否自发进行?。
(2)已知该产业链中某反应的平衡表达式为:
它所对应的化学反应为:。
(3)已知在一定温度下,各反应的平衡常数如下:
C(s)+CO2(g) 2CO(g),K1
2CO(g),K1
CO(g)+H2O(g  H2(g)+CO2(g),K2
H2(g)+CO2(g),K2
C(s)+H2O(g) CO(g)+H2(g),K3
CO(g)+H2(g),K3
则K1、K2、K3之间的关系是:。
(4)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)  H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
| 温度/℃ |
400 |
500 |
800 |
| 平衡常数K |
9.94 |
9 |
1 |
该反应的正反应方向是反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为:。
(5)从图中看出氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等。已知NO2和N2O4的结构式分别是 和
和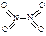 。已知N-N键键能为167kJ·mol-1,NO2中氮氧键的键能为466kJ·mol-1,N2O4中氮氧键的键能为438.5kJ·mol-1。请写出NO2转化为N2O4的热化学方程式为。
。已知N-N键键能为167kJ·mol-1,NO2中氮氧键的键能为466kJ·mol-1,N2O4中氮氧键的键能为438.5kJ·mol-1。请写出NO2转化为N2O4的热化学方程式为。
对反应N2O4(g)  2NO2(g),在温度为T1
2NO2(g),在温度为T1 、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。
、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。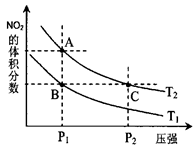
下列说法正确的是 。
A.A、C两 点的反应速率:A>C
点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
(6)以上述产业链中甲醇为燃料制成燃料电池,请写出在氢氧化钾介质中该电池的负极反应式。
[化学—选修5:有机化学基础]
G是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
(1)化合物G的分子式为。B转化为C的反应所属反应类型为。
(2)化合物D的名称为,它的核磁共振氢谱应有组不同类型的峰,它与碳酸氢钠溶液反应的化学方程式为。
(3)化合物E的同分异构体中,能够使三氯化铁溶液显紫色,且能 够水解生成化合物B的有种。这其中核磁共振氢谱图有四组不同类型峰的同分异构体的结构简式为。
够水解生成化合物B的有种。这其中核磁共振氢谱图有四组不同类型峰的同分异构体的结构简式为。
(4)请分别写出A→B、D→E两个转化过程中的反应方程式:、。
【化学——选修3:物质结构与性质】
在A、B、C三种元素中,A元素原子的价电子排布为2s22p5,B元素K、L能层上的电子数与M、N层上的电子数相同。C元素的原子序数等于A、B两元素原子序数之和,C的单质在生产生活中具有许多用途,它可在硫酸铜溶液中用电解法进行精炼。请回答以下问题:
(1)已知C元素的电负性数值为1.9,则A、C两元素的原子之间应形成键(填“共价”或“离子”);
(2)C元素的价电子排布式为____;
(3)在A元素氢化物的水溶液中,存在有种不同类型的氢键;
(4)SO42—中S原子的杂化轨道类型是____,SO42—的立体构型是____;
(5)一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______;该晶体中,原子之间的作用力是________;
(6)在A、B两元素所形成晶体的晶胞中,位于六面体顶点 和面心上的元素为(填具体的元素符号)。
和面心上的元素为(填具体的元素符号)。
【化学——选修2:化学与技术】
水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康。请回答下列问题:
(1)天然水中溶解的气体主要有、。
(2)天然水在净化处理过程中加入的混凝剂可以是,其净水作用的原理是。
(3)水的净化和软化的区别是。
(4)硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO)。若某天然水中c(Ca2+)=1.2×10—3mol/L,c(Mg2+)=6×10—4mol/L,则此水的硬度为。
(5)若(4)中的天然水还含有c(HCO3—)=8×10—4mol/L,现要软化10m3这种天然水,则需先加入Ca(OH)2g,后加入Na2CO3g。