某同学用下列装置制备并检验Cl2的性质。
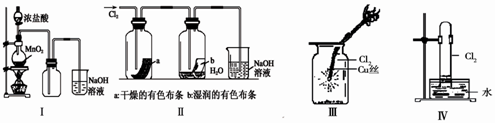
下列说法错误的是( )
| A.Ⅰ图中:即使MnO2过量,盐酸也不能全部消耗 |
| B.Ⅱ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
| C.Ⅲ图中:生成棕色的烟 |
| D.Ⅳ图中:水可以充满试管 |
下列物质加入水中,显著放热的是()
| A.生石灰 | B.固体NaOH | C.无水乙醇 | D.固体硝酸铵 |
山茶油是一种绿色保健食品,其主要成分是柠檬酸,取柠檬酸7.0g,使其在氧气中完全燃烧,只生成22g CO2和7.2g水,没有其他产物,则柠檬酸中( )
| A.含有的元素无法确定 | B.一定含有碳、氢、氧三种元素 |
| C.只含有碳元素 | D.一定含有碳、氢元素,可能含有氧元素 |
取一定质量的下列各组物质混合后,无论以何种比例混合,其充分燃烧后一定能得到相同物质的量的二氧化碳和水的是( )。
| A.C2H2 C2H6 | B.CH4 C3H8 | C.C3H6 C3H8 | D.C2H4 C4H8 |
灰锡(以粉未状存在)和白锡是锡的两种同素异形体。
已知:①Sn(s、白)+2HCl(aq)===SnCl2(aq)+H2(g);ΔH1
②Sn(s、灰)+2HCl(aq)===SnCl2(aq)+H2(g);ΔH2
③Sn(s、灰) 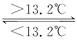 Sn(s、白);ΔH3=+2.1kJ/mol,下列说法正确的是( )
Sn(s、白);ΔH3=+2.1kJ/mol,下列说法正确的是( )
| A.ΔH1>ΔH2 |
| B.锡制器皿长期处于低于13.2℃的环境中,会自行毁坏 |
| C.灰锡转化为白锡的反应是放热反应 |
| D.锡在常温下以灰锡状态存在 |
1mol丙烯与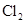 完全加成,其产物再与
完全加成,其产物再与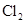 彻底取代,两个过程中共用
彻底取代,两个过程中共用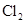 ( )
( )
| A.5mol | B.6mol | C.7mol | D.2mol |