已知一个碳原子上连有两个羟基时,其结构极不稳定,易发生下列变化,生成较稳定物质:如:A﹣F是六种有机化合物,它们之间的关系如图,请根据要求回答:

(1)物质C的结构简式 ,物质D的结构简式 ;
(2)反应③的化学方程式为 .
(3)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n(H2O)=2:1.F是高分子光阻剂生产中的主要原料.F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种.F在一定条件下发生加聚反应的化学方程式为 .
(4)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应G有 种.
有关元素X、Y、Z、W的信息如下:
请回答下列问题:
(1) 写出Y元素在元素周期表的位置。
(2) W的单质与Y的最高价氧化物对应的水化物反应的离子方程式为。
(3) 铜片、碳棒和ZX3溶液组成原电池,写出正极发生的电极反应方程式。
(4) 向淀粉碘化钾溶液中滴加儿滴浓ZX3溶液,现象为,
写出反应的离子方程式。
(5) 以WX3溶液为原料制取WX3·6H20溶液,主要的实验操作是,以WX3·6H20晶体制取无水WX3,应在条件下加热WX3·6H20晶体,其原因是(结合离子方程式简要说明)。
(1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准)。
| 烯类化合物 |
相对速率 |
| (CH3)2C=CHCH3 |
10.4 |
| CH3CH=CH2 |
2.03 |
| CH2=CH2 |
1.00 |
| CH2=CHBr |
0.04 |
据表中数据,总结烯类化合物加溴时,反应速率与C=C上取代基的种类、个数间的关系:
(2)下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是______________(填代号)。
| A.(CH3)2C=C(CH3) 2 | B.CH3CH=CH CH3 |
| C.CH2=CH2 | D.CH2=CHCl |
(3)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3 + HBr → CH3CHBrCH3 + CH3CH2CH2Br
(主要产物) (次要产物)
|
CH2="CH" CH2CH3 + H2O → CH3CH(OH)CH2CH3 + CH3CH2CH2 CH2 OH
(主要产物) (次要产物)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。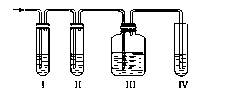
(1)写出实验室制乙烯的反应方程式:
(2)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是:Ⅰ___________;Ⅱ___________;Ⅲ___________;Ⅳ:浓溴水(将下列有关试剂的序号填入空格内)。
| A.品红溶液 | B.NaOH溶液 | C.浓H2SO4 | D.酸性KMnO4溶液 |
(3)能说明二氧化硫气体存在的现象是_______________________________。
(4)确证含有乙烯的现象是_________________________________________。
(5)写出Ⅳ中发生反应的化学方程式:。
写出下列有机物的结构简式:
(1)2,6-二甲基-4-乙基辛烷:;
(2)2-甲基-1-戊烯:;
(3)有A、B、C三种烃,它们的结构简式如下图所示: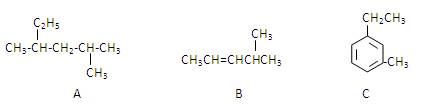
A的名称是;B的名称是;
C的名称是。
选择下列某种答案的序号, 填入下表的空格
①同位素②同素异形体③同分异构体④同系物⑤同种物质
| 物质 |
丁烷与 |
红磷 |
氯仿与 |
氕与 |
新戊烷与 |
| 名称 |
2--甲基丙烷 |
与白磷 |
三氯甲烷 |
氘、氚 |
2,2--二甲基丁烷 |
| 相互 |
|||||
| 关系 |