下列热化学方程式正确的是(ΔH的绝对值均正确)( )
| A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g) ΔH=-1 367.0 kJ·mol-1(标准燃烧热) |
| B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=+57.3 kJ·mol-1(中和热) |
| C.S(s)+O2(g)===SO2(g) ΔH=-296 kJ·mol-1(反应热) |
| D.2NO2===O2+2NO ΔH=+116.2 kJ·mol-1(反应热) |
科学家最近研制出可望成为高效火箭推进剂的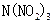 (如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关
(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关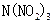 的说法不正确的是
的说法不正确的是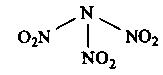
| A.分子中N、O间形成的共价键既有非极性键又有极性健 |
| B.分子中四个氮原子不共平面 |
| C.该物质既有氧化性又有还原性 |
D.15.2g该物质含有6.02×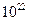 个原子 个原子 |
某无色溶液中可能含有I-、NH+4、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是
①肯定不含I-;②肯定不含Cu2+③肯定含有SO32-④可能含有I-
⑤可能含有SO32-
| A.①②③ | B.②④⑤ | C.①②⑤ | D.②③④ |
120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是
| A.2.0mol/L | B.1.8 mol/L | C.0.18 mol/L | D.0.24mol/L |
X、Y、Z三种短周期非金属元素在元素周期表中的位置如图所示,下列说法正确的是
| A.原子的半径:Y大于Z |
| B.氢化物的稳定性:X高于Y |
| C.高价氧化物水化物的酸性:X大于Y |
| D.原子序数:Z=Y+7 |
某溶液中含有的溶质是FeBr2、FeI2,若先向该溶液中通入一定量的氯气,再向反应后的溶液中滴加KSCN溶液,结果溶液变为红色,则下列叙述不正确的是
| A.原溶液中的Br-一定被氧化 |
| B.通入氯气之后原溶液中的Fe2+一定被氧化 |
| C.不能确定通入氯气之后的溶液中是否存在Fe2+ |
| D.若取少量所得溶液,再加入CCl4溶液,静置、分液,下层溶液呈紫红色 |