电解工作原理的实际应用非常广泛。
(1)电解精炼银时,阴极反应式为____________________________________。
(2)工业上为了处理含有Cr2O72-的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是________
A.阳极反应:Fe-2e-===Fe2+
B.阴极反应:2H++2e-===H2↑
C.在电解过程中工业废水由酸性变为碱性
D.可以将铁电极改为石墨电极
(3)某同学设计了如下图装置进行以下电化学实验。
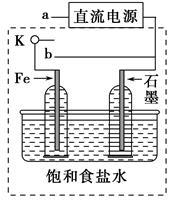
①当开关K与a连接时,两极均有气泡产生,则阴极为_______________极。
②一段时间后,使开关K与a断开、与b连接时,虚线框内的装置可称为__________。
请写出此时Fe电极上的电极反应式__________________。
(4)1 L某溶液中含有的离子如下表:
| 离子 |
Cu2+ |
Al3+ |
NO3- |
Cl- |
| 物质的量浓度( mol·L-1) |
1 |
1 |
a |
1 |
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是________
A.电解后溶液呈酸性
B.a=3
C.阳极生成1.5 mol Cl2
D.阴极析出的金属是铜与铝
核电荷数为1~18的元素中,核外电子总数是原子最外层电子数2倍的元素是______,最外层电子数是次外层电子数2倍的元素是________,次外层电子数是最外层电子数2倍的元素是_________。
在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)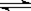 CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =。
(2)该反应为反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
控制变量法是研究化学变化规侓的重要思想方法。请仔细观察下表中50 mL稀盐酸和1g碳酸钙反应的实验数据:
| 实验 序号 |
碳酸钙 状态 |
c(HCl) /mol·L-1 |
溶液温度/℃ |
碳酸钙消失 时间/s |
|
| 反应前 |
反应后 |
||||
| 1 |
粒状 |
0.5 |
20 |
39 |
400 |
| 2 |
粉末 |
0.5 |
20 |
40 |
60 |
| 3 |
粒状 |
0.6 |
20 |
41 |
280 |
| 4 |
粒状 |
0.8 |
20 |
40 |
200 |
| 5 |
粉末 |
0.8 |
20 |
40 |
30 |
| 6 |
粒状 |
1.0 |
20 |
40 |
120 |
| 7 |
粒状 |
1.0 |
30 |
50 |
40 |
| 8 |
粒状 |
1.2 |
20 |
40 |
90 |
| 9 |
粒状 |
1.2 |
25 |
45 |
40 |
分析并回答下列问题:
(1)本反应属于________反应(填“吸热”或“放热”),反应的离子方程式为。
(2)实验6和7表明,_________对反应速率有影响,_________反应速率越快,能表明同一规律的实验还有_________(填实验序号)。
(3)根据实验1、3、4、6、8可以得出条件对反应速率的影响规律是。
(4)本实验中影响反应速率的其它因素还有__________,能表明这一规律的实验序号是1、2与_______。
下列物质中:①NaCl ②Na2O ③CH3COOH ④CO2 ⑤NaHCO3 ⑥NH3·H2O ⑦HCl ⑧NaOH ⑨Cl2 ⑩酒精 请按要求回答下列问题(填编号):
(1) 属于电解质的有 ;(2)属于非电解质的有: ;
(3)属于强电解质的有;(4)属于弱电解质的有;
(5)请分别写出NH3·H2O ,NaHCO3的电离方程式:;。
硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。 已知:①Fe3+、Al3+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2和12.4;Al(OH)3完全溶解的pH为11.8。②常温下,饱和氨水的pH约为11。
已知:①Fe3+、Al3+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2和12.4;Al(OH)3完全溶解的pH为11.8。②常温下,饱和氨水的pH约为11。
请回答:(1)写出A与氢氧化钠溶液反应的化学方程式:。
(2)上述流程中试剂②应该是(填以下字母编号)。
| A.氢氧化钠 | B.氧化铝 | C.氨水 | D.水 |
(3)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是
。
(4)计算溶液F中c(Mg2+)=( 25℃时,氢氧化镁的Ksp=5.6×10-12)。
(5)工业生产中将固体C灼烧后的产物与KNO3、KOH固体加热共熔制备净水剂K2FeO4,同时获得一种亚硝酸盐,请写出制得K2FeO4的化学方程式:。