下列各溶液中微粒的物质的量浓度关系错误的是( )
A.0.2mol/L K2CO3溶液中c(OH-)=c(HCO-3)+c(H+)+2c(H2CO3)
B.0.1mol/L NaHA溶液中其中pH=3,c(HA-)>c(H+)>c(H2A)>c(A2-)
C.向Na2SO4溶液中滴加稀CH3COOH得到pH=4的混合溶液c(Na+)=2c(SO42-)
D.pH=a的HA溶液与pH=b的MOH溶液任意比混合c(H+)+c(M+)=c(OH-)+c(A-)
下列曲线中,可以描述乙酸(甲,Ka=1.8×10-5)和一氯乙酸(乙,Ka=1.4×10-3)在水中的电离度与浓度关系的是
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 |
实 验 |
现 象 |
结 论 |
| A. |
将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 |
有气体生成,溶液呈血红色 |
稀硝酸将Fe氧化为Fe3+ |
| B. |
将铜粉加1.0 mol·L-1 Fe2(SO4)3溶液中 |
溶液变蓝、有黑色固体出现 |
金属铁比铜活泼 |
| C. |
用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 |
熔化后的液态铝滴落下来 |
金属铝的熔点较低 |
| D. |
将0.1mol·L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol·L-1CuSO4溶液 |
先有白色沉淀生成后变为浅蓝色沉淀 |
Cu(OH)2的溶度积比Mg(OH)2的小 |
下列有关NaClO和NaCl混合溶液的叙述正确的是
| A.该溶液中,H+、NH4+、SO42-、Br-可以大量共存 |
| B.该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存 |
| C.向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+=== Cl-+2Fe3++H2O |
| D.向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为
| A.C14H18O5 | B.C14H16O4 | C.C14H22O5 | D.C14H10O5 |
下列三种有机物是某些药物中的有效成分: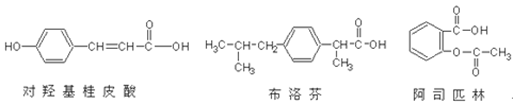
以下说法不正确的是
| A.三种有机物都属于芳香烃化合物 |
| B.三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种 |
| C.将各1mol的三种物质分别与氢氧化钠溶液充分反应,阿司匹林消耗氢氧化钠最多 |
| D.三种有机物都能与浓溴水发生反应 |