在锌片和盐酸的反应中,加入如下试剂,可使生成氢气的速度变慢的是 ( )
| A.硫酸铜晶体 | B.HCl气体 | C.氯化钡晶体 | D.醋酸钾晶体 |
用石墨作电极,电解1 mol/L下列物质的溶液,溶液的pH保持不变的是
| A.HCl | B.NaOH | C.Na2SO4 | D.NaCl |
在恒温恒压的密闭容器中,充入 4L X和3L Y的混合气体,在一定条件下发生下列反应:
4X(g)+3Y(g) 2Q(g)+ nR(g)达到平衡时测得 X的转化率为 25%,此时混合气体的体积为6.5L。则该反应方程式中的n值是
2Q(g)+ nR(g)达到平衡时测得 X的转化率为 25%,此时混合气体的体积为6.5L。则该反应方程式中的n值是
| A.8 | B.6 | C.5 | D.3 |
在密闭容器中,一定量混合气体发生下列反应: aM(g)+ bN(g) cW(g),达一平衡后,测得M气体的浓度为0.5mol/L。当在恒温下,将密闭容器的体积扩大1倍,再达平衡时,测得M气体的浓度为0.3mol/L。则下列叙述正确的是
cW(g),达一平衡后,测得M气体的浓度为0.5mol/L。当在恒温下,将密闭容器的体积扩大1倍,再达平衡时,测得M气体的浓度为0.3mol/L。则下列叙述正确的是
| A.反应速率增大 | B.平衡向右移动 |
| C.N的转化率提高 | D.W的体积分数降低 |
在真空恒容密闭容器中盛有1 mol PCl5加热到200℃时发生的如下反应:
PCl5(气)  PCl3(气) +Cl2(气),反应达平衡后,PCl5所占体积分数为M%。若在同一温度和同一容器中,最初投入的是2 mol PCl5(气),反应达平衡时,PCl5所占体积分数为 N%。则M和N的正确关系是
PCl3(气) +Cl2(气),反应达平衡后,PCl5所占体积分数为M%。若在同一温度和同一容器中,最初投入的是2 mol PCl5(气),反应达平衡时,PCl5所占体积分数为 N%。则M和N的正确关系是
| A.M>N | B.M<N | C.M="N" | D.无法比较 |
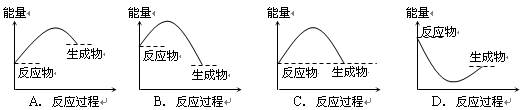
下列各图所表示的反应是吸热反应的是