空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是( )
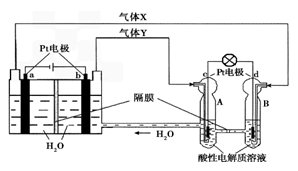
A.当有0.1 mol电子转移时,a极产生1.12 L O2(标况)
B.b极上发生的电极反应是:2H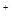 + 2e- = H2↑
+ 2e- = H2↑
C.d极上发生的电极反应是:O2 + 4H+ + 4e- = 2H2O
D.c极上进行还原反应,B中的H+可以通过隔膜进入A
一定条件下,用甲烷可以消除氮的氧化物(NOx)的污染。已知:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160 kJ·mol-1
下列选项正确的是
| A.CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1 |
| B.CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g) ΔH=+1734 kJ·mol-1 |
| C.CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l)ΔH=-x kJ·mol-1 x <574 |
| D.常温常压下用2.24 L CH4还原NO2至N2,整个过程中转移的电子为0.8 mol |
已知2SO2(g)+O2(g)  2SO3 (g)△H =-a kJ·mol-1(a>0)。恒温恒容下,在10L的密闭容器中加入0.1molSO2和0.05molO2,经过2min达到平衡状态,反应放热0. 025a kJ。下列判断正确的是
2SO3 (g)△H =-a kJ·mol-1(a>0)。恒温恒容下,在10L的密闭容器中加入0.1molSO2和0.05molO2,经过2min达到平衡状态,反应放热0. 025a kJ。下列判断正确的是
| A.在2min内,v (SO2)="0.25" mol·L-1·min-1 |
| B.若再充入0.1molSO3,达到平衡后SO3的质量分数会减小 |
| C.在1min时,c(SO2)+c(SO3)="0.01" mol·L-1 |
| D.若恒温恒压下,在10L的密闭容器中加入0.1molSO2和0.05molO2,平衡后反应放热小于0. 025a kJ |
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X形成的最高价氧化物对应的水化物的碱性强于Y。下列说法正确的是
| A.原子半径大小为Z>Y>X>W |
| B.W与X形成的化合物中可能含有共价键 |
| C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
用NA表示阿伏加德罗常数值,下列叙述正确的是
| A.1 molNa2O2与足量的水反应,转移的电子数为2NA |
| B.7.1 g Cl2完全参加反应,转移的电子数一定为0.1NA |
| C.电解饱和食盐水,生成1mol氢氧化钠,转移的电子数为2 NA |
| D.标准状况下,22.4L的CO2和O2组成的混合物中,含氧原子数为2NA |
已知实验室中,可用Co2O3代替MnO2来制备氯气,反应前后存在的六种微粒分别是:Co2O3、H2O、Cl2、H+、Cl-和Co2+。下列叙述不正确的是
| A.Cl2发生还原反应 |
| B.氧化剂与还原剂的物质的量之比为1︰2 |
| C.若反应中生成3molH2O,则转移电子2mol |
| D.理论上利用该反应可以将化学能转化为电能 |