为了配制NH4+的浓度与Cl-的浓度比为1:1的溶液,可在NH4Cl溶液中加入适量( )
①浓盐酸 ②NaCl固体 ③浓氨水 ④ NaOH固体
| A.①② | B.③ | C.③④ | D.④ |
已知分子式为C12H12的物质A的结构简式为 ,其苯环上的二溴代物有9种同分 异构体,由此推断A苯环上的四溴代物的同分异构体的数目有()
,其苯环上的二溴代物有9种同分 异构体,由此推断A苯环上的四溴代物的同分异构体的数目有()
| A.9种 | B.10种 | C.11种 | D.12种 |
某烯烃氢化后得到的饱和烃是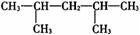 ,则原烯烃可能有的结构简式有
,则原烯烃可能有的结构简式有
| A.1种 | B.2种 | C.3种 | D.4种 |
已知甲、乙两种烃含碳的质量分数相同,下列判断正确的是
| A.甲和乙一定是同分异构体 |
| B.甲和乙的实验式一定相同 |
| C.甲和乙不可能是同系物 |
| D.等物质的量的甲和乙完全燃烧后生成水的质量一定相等 |
NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1mol乙醇中含有C—H键的数目为4NA |
| B.常温常压下,44 g C3H8中含有的碳碳单键数为3NA |
| C.2.3g C7H8和C3H8O3的混合物中,含氢原子数目为0.2NA |
| D.标准状况下,2.24 L溴乙烷中含共价键数目为0.7NA |
已知正四面体形分子E和直线型分子G反应,生成四面体形分子L和双原子分子M。(组成E分子的元素的原子序数都小于10,组成G分子的元素为第三周期的元素。)如下图,则下列判断中正确的是
(E) (G) (L) (M)
| A.常温常压下,L是一种液态有机物 | B.E中化学键是极性键 |
| C.G有漂白性 | D.上述反应的类型是加成反应 |