已知反应:① 2C(s)+O2(g)=2CO(g) ΔH1=-221 kJ/mol
②CO(g)+1/2O2(g)=CO2(g) ΔH2=-283 kJ/mol
③稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH3=-57.3 kJ/mol
下列结论正确的是
| A.12gC燃烧生成CO时,放出221 kJ热量 |
| B.碳的燃烧热ΔH=-393.5 kJ/mol |
| C.CO(g)+1/2O2(g)=CO2(s)ΔH > ΔH2 |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水时,放出57.3 kJ 热量 |
在aLAl2(SO4)3和(NH4)2SO4的混合溶液中加入bmol的BaCl2,恰好使溶液中的SO42-完全沉淀;如加入足量强碱并加热可得到cmolNH3,则原溶液中的Al3+的浓度(mol/L)为
A.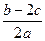 |
B.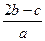 |
C.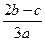 |
D.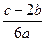 |
下列溶液中有关物质的量浓度关系正确的是
A.0.2 mol/L的NaHCO3溶液: c(HCO3-)>c(CO32-)>0.1 mol/L>c(H2CO3) c(HCO3-)>c(CO32-)>0.1 mol/L>c(H2CO3) |
B.pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合: c(Na+)>c(CH3COO-)>c(OH-)>c(H+) c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
C.0.2 mol/L CH3COOH溶液和0.2 mol/L CH3COONa溶液等体积混合: c(CH3COO-)+c(OH-)-c(H+)=0.1 mol/L c(CH3COO-)+c(OH-)-c(H+)=0.1 mol/L |
D.0.1mol/LNa2CO3溶液与0.1mol/LNaHCO3溶液等体积混合 |
 c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+)
c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+)
在下列溶液中,各组离子一定能够大量共存的是
A.pH=2的溶液: Fe3+、Cu2+、SO42-、NO3- |
B.c(H+)=1×10-12mol/L的溶液:NH4+、K+、Cl-、AlO2- |
C.水电离的c(H+)=1×10-12mol/L的溶液:Na+、Al3+、Br-、ClO-  |
D.与铝反应放出氢气的溶液:Na+、Mg2+、Br-、Cl- |
科学家研制出多种新型杀虫剂代替DDT,化合物A是其中一种。下列关于化合物A的说法正确的是
A.与FeCl3溶液发生反应显紫色 |
B.能发生取代反应和银镜反应 |
C.分子中最多有5个碳原子共平面 |
D.与H2完全加成时的物质的量之比为1∶1 |
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是



| A.将海带灼烧成灰 | B.过滤得含I-溶液 | C.放出碘的苯溶液 | D.分离碘并回收苯 |