已知如下两个热化学反应方程式:


下列说法不正确的是 ( )
| A.反应①、②都属于加成反应 |
| B.反应①吸热、反应②放热的事实说明苯环中含有的并不是碳碳双键 |
| C.反应①、②中的所有有机物均可使溴水褪色,但褪色原理不完全相同 |
| D.在通常条件下,反应①、②都能自发进行 |
一个固定体积的密闭容器中,加入2molA和1molB,发生反应2A(g)+B(g) 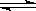 3C(g)+D(s),达到平衡时,C的浓度为ω mol/L。若维持容器体积和温度不变,改由下列四种配比作为起始物质,达到平衡时,C的浓度仍为ω mol/L的是
3C(g)+D(s),达到平衡时,C的浓度为ω mol/L。若维持容器体积和温度不变,改由下列四种配比作为起始物质,达到平衡时,C的浓度仍为ω mol/L的是
| A.4molA+2molB | B.3molC+2molD |
| C.1molB+3molC+1molD | D.2molA+1molB+3molC+1molD |
右图表示298K时N2与H2反应过程中的能量变化。根据右图叙述正确的是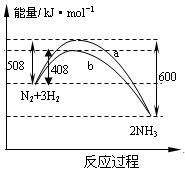
A.该反应的热化学方程式为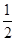 N2(g)+ N2(g)+ 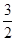 H2(g) H2(g) NH3(g),△H=-92kJ·mol-1 NH3(g),△H=-92kJ·mol-1 |
| B.不用催化剂,生成 1molNH3放出的热量为46 KJ |
| C.加入催化剂,生成 1molNH3的反应热减小50 KJ·mol-1 |
| D.曲线b表明加入催化剂降低了反应热,加快了反应速率 |
用惰性电极电解足量下列溶液,一段时间后,再加入一定质量的另一种物质(括号内),溶液能与原来溶液完全一样的是
| A.CuCl2 [CuCl2溶液] | B.NaOH [NaOH溶液] |
| C.NaCl [HCl气体] | D.CuSO4 [Cu(OH)2] |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是
| A.放电时负极反应为:3Zn-6e-+6OH-==3Zn(OH)2 |
B.充电时阳极反应为:Fe(OH)3-3e-+5OH- FeO42- +4H2O FeO42- +4H2O |
| C.放电时每转移3 mol电子,正极有1 mol K2FeO4被还原 |
| D.充电时阴极溶液的碱性减弱 |
乙苯催化脱氢制苯乙烯反应: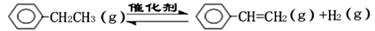
已知:1 mol C-H键完全断裂时吸收热量412kJ,1 mol C-C键完全断裂时吸收热量348kJ
1 mol C=C键完全断裂吸收热量612kJ,1 mol H-H键完全断裂时吸收热量436kJ。
上述反应的△H等于kJ·mol-1。
| A.-124 | B.+124 | C.-288 | D.+288 |