高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。下列反应可制取K2FeO4:
2 Fe(OH)3 +3 Cl2+10KOH 0~30℃ 2 K2FeO4+6KCl+8H2O,对于该反应,下列说法正确的是
| A.水是还原产物 | B.Fe(OH)3发生还原反应 |
| C.Cl2是氧化剂 | D.每生成1mol K2FeO4转移2mol电子 |
在许多化合物里硫可以取代氧,取代后的物质跟原化合物有相似的性质,下面是两种有机磷农药的结构:
①
②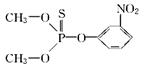
这两种农药在使用过程中不能与下列哪种物质混合使用( )
| A.KCl | B.NaOH | C.NaNO3 | D.Na2SO4 |
据报道我国科学家最近研制出一种新型“连续纤维增韧”航空材料,其主要成分是由碳化硅、陶瓷和碳纤维复合而成。下列相关叙述不正确的是( )
| A.它耐高温抗氧化 |
| B.它比钢铁轻、硬,但质地较脆 |
| C.它没有固定熔点 |
| D.它是一种新型无机非金属材料 |
我们看到的普通玻璃一般呈淡绿色,这是因为在制造玻璃的过程中加入了( )
| A.氧化钴 | B.二价铁 |
| C.氧化亚铜 | D.氧化镁 |
下列说法错误的是( )
| A.制造水泥和玻璃都用到的原料是CaCO3 |
| B.为了调节水泥的硬化速度,制造水泥时需要加入石膏 |
| C.当水泥、沙子与水调成水泥浆时,水泥浆对皮肤有腐蚀作用,这是因为水泥浆呈较强的碱性 |
| D.水泥、玻璃、陶瓷都是混合物,具有较高的熔点 |
光导纤维是一种新型的通讯材料。具有信息量大、质量小、性能好、成本低的特点。每根光纤理论上可同时通过10亿路电话,不怕腐蚀、抗电磁干扰、保密性强;每公里仅有27 g,仅1万元左右。制造光导纤维的主要原料是( )
| A.晶体硅 | B.二氧化硅 |
| C.石墨 | D.二氧化锗 |