在海轮的船壳上连接锌块,下列相关说法正确的是
| A.制成合金保护船体 | B.是外加电流的阴极保护法 |
| C.船体的反应:Fe -2e → Fe2+ | D.锌块的反应:Zn -2e → Zn2+ |
水钴矿(含CuO、Co2O3、Fe2O3、MgO等)用硫酸法浸出铜和钴,下图是不同还原剂对元素浸出率的影响(硫酸的浓度3 mol•L-1,温度60℃),下列说法正确的是
| A.是否使用还原剂对铜的浸出率影响很大 |
| B.用Na2SO3、NaNO2作还原剂,钴的浸出率 均达98%,但工业上宜选用Na2SO3 |
| C.加入还原剂的主要目的是为了还原Fe3+ |
| D.用Na2SO3作还原剂可使镁元素以单质 形式析出而有较大浸出率 |
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是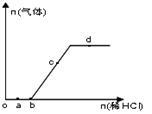
| A.a点对应的溶液中:Na+、OH-、SO42-、NO3- |
| B.b点对应的溶液中:K+、OH-、MnO4-、Cl- |
| C.c点对应的溶液中:Na+、Ca2+、NO3-、Cl- |
| D.d点对应的溶液中:K+、Fe2+、NO3-、SO42- |
120mL含有0.20mol碳酸钠的溶液和200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是
| A.2.0mol/L | B.1.5mol/L | C.0.18mol/L | D.0.24mol/L |
下列离子方程式不正确的是
| A.NaHSO4溶液中加入过量Ba(OH)2溶液:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| B.次氯酸钙溶液中加入亚硫酸钠:SO32-+Ca2+=CaSO3↓ |
C.NH4HCO3溶液中加足量NaOH溶液共热:HCO3-+NH4++2OH- CO32-+NH3↑+2H2O CO32-+NH3↑+2H2O |
| D.硫酸亚铁溶液中加入用硫酸酸化的双氧水:2Fe2++2H++H2O2=2Fe3++2H2O |
将0.51mol铜与250mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L.待产生的气体全部释放后,向溶液中加入300mL5mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀.则下列选项正确的是
| A.产生NO气体0.24mol | B.产生NO2气体0.26mol |
| C.原HNO3浓度为8mol/L | D.原HNO3浓度为2mol/L |