常温下0.1 mol/L醋酸溶液的pH = a,下列能使溶液pH =(a +1)的措施是
| A.将溶液稀释到原体积的10倍 |
| B.加入适量的醋酸钠固体 |
| C.加入等体积0.1 mol/L烧碱溶液 |
| D.加入等体积0.1 mol/L盐酸 |
某种氢气和CO的混合气体,其密度是氧气的一半,则氢气的体积百分含量约为
| A.40% | B.46% | C.50% | D.54% |
如图所示装置,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于
| A.2:7 | B.5:4 | C.4:5 | D.7:3 |
下列化学实验操作或事故处理方法正确的是
| A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硫酸 |
| C.酒精灯着火时可用水扑灭 |
| D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸 |
质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水.得到的溶液每毫升质量为q g,物质的量浓度为c.则溶质的分子量(相对分子质量)为
A.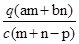 |
B.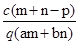 |
C.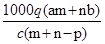 |
D.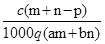 |
若20 g密度为ρ g·cm-3的硝酸钙溶液里含1 g Ca2+,则NO的物质的量浓度是
A.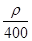 mol·L-1 mol·L-1 |
B.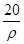 mol·L-1 mol·L-1 |
| C.2.5ρmol·L-1 | D.1.25ρmol·L-1 |