下列实验所采取的分离方法与对应原理都正确的是
| 选项 |
目的 |
分离方法 |
原理 |
| A |
提取碘水中的碘 |
乙醇萃取 |
碘在乙醇中溶解度比水中大 |
| B |
除去纯碱中的碳酸氢铵 |
加热 |
纯碱热稳定性大于碳酸氢铵 |
| C |
分离KNO3和NaCl |
重结晶 |
KNO3的溶解度大于NaCl |
| D |
分离乙酸乙酯和乙醇 |
分液 |
乙酸乙酯密度大于乙醇 |
某有机物X能发生水解反应,水解产物为Y和Z。同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是( )
| A.乙酸丙酯 | B.甲酸乙酯 |
| C.乙酸甲酯 | D.乙酸乙酯 |
下列物质的浓溶液中滴入盐酸后,溶液变浑浊的是( )
| A.C2H5OH |
| B.AgNO3 |
C. |
| D.Na2CO3 |
2002年瑞典科学家发现,某些高温油炸食品中含有一定量的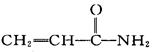 (丙烯酰胺)。食品中过量的丙烯酰胺可能引起令人不安的食品安全问题。关于丙烯酰胺有下列叙述: ①能使KMnO4酸性溶液褪色,②能发生加聚反应生成高分子化合物,③只有4种同分异构体,④能与氢气发生加成反应。其中正确的是( )
(丙烯酰胺)。食品中过量的丙烯酰胺可能引起令人不安的食品安全问题。关于丙烯酰胺有下列叙述: ①能使KMnO4酸性溶液褪色,②能发生加聚反应生成高分子化合物,③只有4种同分异构体,④能与氢气发生加成反应。其中正确的是( )
| A.①②③ | B.②③④ |
| C.①③④ | D.①②④ |
漆酚是我国特产生漆的主要成分,其中一种的结构简式为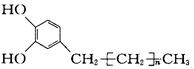 生漆涂在物体表面,在空气中干燥时会产生黑色漆膜,则漆酚不应具有的化学性质是( )
生漆涂在物体表面,在空气中干燥时会产生黑色漆膜,则漆酚不应具有的化学性质是( )
| A.可以与烧碱溶液反应 |
| B.可以与溴水发生取代反应 |
| C.可使KMnO4酸性溶液褪色 |
| D.可与NaHCO3溶液反应放出二氧化碳 |
胆固醇是人体必需的生物活性物质,分子式为C27H46O。一种胆固醇酯是液晶材料,分子式为 C34H50O2 。生成这种胆固醇酯的酸是 ( )
| A.C6H13COOH |
| B.C6H5COOH |
| C.C7H15COOH |
| D.C6H5CH2COOH |