下表中对陈述I、II的正确性及两者间是否具有因果关系的判断都正确的是()
| |
陈述I |
陈述II |
判断 |
| A |
Fe3+具有氧化性 |
用KSCN溶液可以鉴别Fe3+ |
I对,II对,有 |
| B |
溶解度:CaCO3<Ca(HCO3)2 |
溶解度Na2CO3<NaHCO3 |
I对,II对,无 |
| C |
金属钠具有强氧化性 |
高压钠灯发出透雾性强的黄光 |
I对,II对,有 |
| D |
SiO2可与HF反应 |
氢氟酸不能保存在玻璃瓶中 |
I对,II对,有 |
要证明一氯甲烷中氯元素的存在可以进行如下操作,其中顺序正确的是()
①加入AgNO3溶液②加入NaOH水溶液③加热④加蒸馏水⑤冷却后加入HNO3酸化⑥加入NaOH的乙醇溶液
| A.④③①⑤ | B.②③⑤① | C.⑥③④① | D.⑥③⑤① |
下列说法正确的是()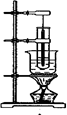

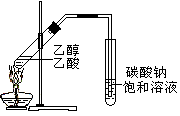
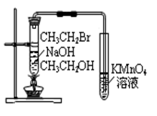
图1图2图3图4
| A.图1为实验室制备硝基苯的装置 |
| B.图2中振荡后下层为无色 |
| C.制备乙酸乙酯:用右图所示的实验装置 |
| D.图4装置可以达到验证溴乙烷发生消去反应生成烯烃的目的 |
右图表示4-溴环己烯所发生的4个不同反应。其中,产物官能团种类不会减少的反应是( )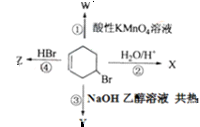
| A.②③ | B.③④ |
| C.①② | D.①④ |
由乙炔和乙醛组成的混和气体,经测定其中碳的质量分数是72%,则混和气体中氧的质量分数是()
| A.32.33% | B.22.65% | C.19.56% | D.2.14% |
2008年北京残奥会吉祥物是“福牛乐乐”。有一种有机物的键线式也酷似牛形(如图所示),故称为牛式二烯炔醇。下列有关牛式二烯炔醇的说法中正确的是 ( )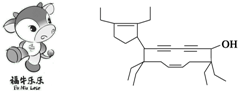
| A.化学式为C29H44O,属于不饱和醇 |
| B.分子内所有碳原子都在同一平面 |
| C.能发生加成、消去、取代反应 |
| D.一定条件下羟基能被氧化为醛基 |