设NA为阿伏加德罗常数的值,下列说法不正确的是
| A.物质的量浓度为1 mol/L的K2SO4溶液中,含2 mol K+ |
| B.把40 g NaOH固体溶于水得到1 L溶液,所得溶液中NaOH的物质的量浓度为1 mol·L-1 |
| C.常温常压下,71 g Cl2含有2 NA个Cl原子 |
| D.标准状况下,11.2 L N2中含有的电子数为7NA |
下列反应中,属于氧化还原反应的是
A.2 H2O2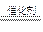 2 H2O + O2↑ 2 H2O + O2↑ |
B.2 Al(OH)3 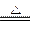 Al2O3 + 3 H2O Al2O3 + 3 H2O |
| C.FeO + 2 HCl = FeCl2+ H2O | D.FeCl2 + 2 NaOH =" Fe" (OH)2↓+ 2NaCl |
下列各组物质混合后,不能生成NaOH的是
| A.Na和H2O | B.Ca(OH)2溶液和NaCl溶液 |
| C.Na2O2和H2O | D.Ca(OH)2溶液和Na2CO3溶液 |
关于Al的叙述中,正确的是
| A.Al的摩尔质量是27 g | B.1mol Al中所含原子数约为6.02×1023 |
| C.1 mol Al的质量是27 g / mol | D.常温常压下,1 mol Al的体积为22.4 L |
下列离子方程式书写正确的是
| A.氧化铝粉末投入NaOH溶液中: Al2O3+2OH-=2AlO2-+H2↑ |
| B.金属钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ |
| C.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| D.氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
下列各组中的离子,能在溶液中大量共存的是
| A.H+、Na+、CO32- | B.Cl-、Ba2+、SO42- |
| C.Fe3+、OH-、SO42- | D.H+、Ag+、NO3- |