将淀粉浆和淀粉酶的混合物放入半透膜中,扎好,浸入流动的温水中,过相当一段时间后,取出袋中的液体,使之分别与碘水,新制的氢氧化铜(加热),浓硝酸接触,可观察到的现象是:
| A.显蓝色,无现象,显黄色 | B.显蓝色,有红色沉淀,无现象 |
| C.无现象,凝结,显黄色 | D.无现象,有红色沉淀,显黄色 |
将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是()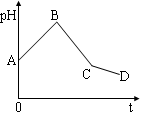
| A.阳极产物一定是Cl2,阴极产物一定是Cu |
| B.BC段表示在阴极上是H+放电产生了H2 |
| C.整个过程中阳极先产生Cl2,后产生O2 |
| D.CD段表示阳极上OH一放电破坏了水的电离平衡,产生了H+ |
设NA为阿伏加德罗常数的值,下列叙述不正确的()
| A.10g质量分数为46%的乙醇溶液中,氢原子的总数为0.6NA |
| B.5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA |
| C.50 mL 12 mol•L-1浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| D.常温常压下,46g NO2 与N2O4的混合气体中含有的原子总数为3NA |
下列有关化学用语使用正确的是()
A.CO2的电子式: |
| B.次氯酸的结构式: H—O—Cl |
C.中子数为18的氯原子结构示意图: |
| D.二氧化硅的分子式为:SiO2 |
下列分类或归类正确的是( )
①液氯、氨水、干冰、碘化银均为纯净物
②CaCl2、NaOH、HCl、IBr均为化合物
③明矾、水银、烧碱、硫酸均为强电解质
④C60、C70、金刚石、石墨均为碳的同素异形体
⑤碘酒、淀粉、水雾、纳米材料均为胶体
| A.①③④ | B.②③ | C.②④ | D.②③④⑤ |
化合物A、B、C、D各由两种元素组成,甲、乙、丙是短周期元素的三种单质。这些常见的化合物与单质之间存在如下关系(已知C是一种有机物),以下结论不正确的()
A.甲、乙、丙三种单质的晶体一定是分子晶体
B.上述转化关系所涉及的化合物中有一种是电解质
C.上图所示的五个转化关系中,有三个是化合反应
D.上图所示的五个转化关系中,均为氧化还原反应