下列有关热化学方程式的叙述正确的是
| A.已知2H2(g)+O2(g)=2H2O(g) △H =-483.6kJ·mol-1,则氢气的标准燃烧热为-483.6kJ/mol |
| B.ΔH的数值与化学反应方程式的化学计量系数无关 |
| C.含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则该反应的热化学方程式为:NaOH(aq)+1/2H2SO4(aq)=1/2Na2SO4(aq)+H2O(l) △H =-57.4 kJ·mol-1 |
| D.己知C(s)+O2(g)=CO2(g) △H1;C(g)+O2(g)=CO2(g) △H2,则△H1﹤△H2 |
某高分子化合物的部分结构如下: 下列说法中正确的是( )
下列说法中正确的是( )
| A.若n为聚合度,则该物质的相对分子质量为97n |
B.该聚合物的链节是 |
| C.该聚合物的化学式为(C3H3Cl3)n |
| D.单体是CH2===CHCl |
生成高聚物 的单体有( )
的单体有( )
| A.1种 | B.2种 |
| C.3种 | D.4种 |
下列关于乙烯和聚乙烯的叙述中正确的是( )
| A.二者都能使溴水褪色,性质相似 |
| B.二者互为同系物 |
| C.二者最简式相同 |
| D.二者分子组成相同 |
核黄素又称维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳,核黄素分子的结构为:
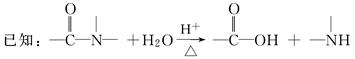
有关核黄素的下列说法中,不正确的是( )
| A.该化合物的分子式为C17H22N4O6 |
| B.酸性条件下加热水解,有CO2生成 |
| C.酸性条件下加热水解,所得溶液加碱后有NH3生成 |
| D.能发生酯化反应 |
速效感冒冲剂的主要成分之一为“对酰基酚”,其结构简式为: 有关它的叙述不正确的是( )
有关它的叙述不正确的是( )
| A.能溶于热水 |
| B.在人体内分解 |
| C.1 mol对酰基酚与溴水反应时最多消耗Br2 4 mol |
| D.与硝基乙苯互为同分异构体 |