等质量的两份锌粉a、b分别加到两份质量相同的过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,下列各图为产生H2的体积V(L)与时间t(min)的关系,其中正确的是
如图所示a、b都是惰性电极,通电一段时间后,a极附近溶液显红色。下列说法中正确的是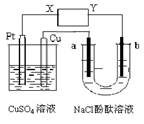
| A.X是正极,Y是负极 |
| B.X是负极,Y是正极 |
| C.CuSO4溶液的浓度逐渐减小 |
| D.CuSO4溶液的pH减小 |
用0.10 mol/L 的盐酸滴定0.10 mol/L 的氨水,滴定过程中不可能出现的结果是
A.c(NH4+)>c(Cl ),c(OH ),c(OH )>c(H )>c(H ) ) |
B.c(NH4+) = c(Cl ),c(OH ),c(OH ) = c(H ) = c(H ) ) |
C.c(Cl )>c(NH4+),c(OH )>c(NH4+),c(OH )>c(H )>c(H ) ) |
D.c(Cl )>c(NH4+),c(H )>c(NH4+),c(H )>c(OH )>c(OH ) ) |
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH +  2H2O
2H2O Cd(OH)2
Cd(OH)2
+ 2Ni(OH)2。有关该电池的说法正确的是
| A.充电时阳极反应:Ni(OH)2-e-- + OH-- ="=" NiOOH + H2O |
B.充电过程是化学能转化为电能 的过程 的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
常温下,某溶液中由水电离的c(H +)=1×10-13 mol/L,该溶液可能是
+)=1×10-13 mol/L,该溶液可能是
①二氧化硫水溶液②氯化铵水溶液 ③硝酸钠水溶液④氢氧化钠水溶液
| A.①④ | B.①② | C.②③ | D.③④ |
下列关于热化学反应的描述中正确的是
A.HCl和NaO H反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol H反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| B.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的 |
△H=2×283.0kJ/mol