为了验证NaHCO3固体中是否含有Na2CO3,下列实验及判断中,正确的是
| A.在试管中加热,观察是否有气体放出 |
| B.溶于水后加BaC12,看有无沉淀 |
| C.溶于水后加石灰水,看有无沉淀 |
| D.取固体试样加盐酸,看是否有气泡产生 |
物质的量浓度相同的下列溶液中,NH+4浓度最大的是( )
| A.NH4Cl | B.NH4HSO4 |
| C.CH3COONH4 | D.NH4HCO3 |
用水稀释0.1 mol·L-1氨水时,溶液中随着水量的增加而减小的是( )
| A.c(OH-)/c(NH3·H2O) |
| B.c(NH3·H2O)/c(OH-) |
| C.c(H+)和c(OH-)的乘积 |
| D.OH-的物质的量 |
在医院中,为酸中毒病人输液不应采用( )
| A.0.9%氯化钠溶液 | B.0.9%氯化铵溶液 |
| C.1.25%碳酸氢钠溶液 | D.5%葡萄糖溶液 |
把3体积的NO2气体,依次通过下列3个分别装有①NaHCO3饱和溶液②浓H2SO4③Na2O2的装置,用排水法把残留气体收集到集气瓶中,集气瓶内气体应是(同温同压下测定)()
| A.1体积NO |
| B.2体积NO2和0.5体积O2 |
| C.2体积O2 |
| D.0.25体积O2 |
已知反应aR2O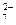 +xM2++14H+====bR3++xM3++cH2O,则化学计量数x的值是()
+xM2++14H+====bR3++xM3++cH2O,则化学计量数x的值是()
| A.6 | B.2 | C.4 | D.3 |