下列实验操作或对实验事实的叙述中存在错误的是( )
| A.用50 mL酸式滴定管准确量取25.00 mL酸性KMnO4溶液,放入锥形瓶中待用 |
| B.室温下,测定浓度为0.1 mol·L-1 NaClO溶液和0.1 mol·L-1CH3COONa溶液的pH,比较HClO和CH3COOH的酸性强弱 |
| C.实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉 |
| D.配制1 mol·L-1的NaOH溶液时,若容量瓶中原有少许蒸馏水会造成所配浓度偏低 |
下列关于化学键的说法正确的是
A.C、N、O、H四种元素形成的化合物一定既有离子键,又有共价键
B.不同元素的原子构成的分子不一定只含极性共价键
C.含极性键的共价化合物一定是电解质
D.HF的分子间作用力大于HCl,故HF比HCl更稳定
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊醋的结构简式如图:下列对该化合物叙述正确的是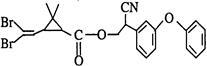
| A.属于芳香烃 |
| B.属于卤代烃 |
| C.在酸性条件下不水解 |
| D.在一定条件下可以发生加成反应 |
有4种有机物:①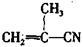 ②
②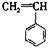 ③
③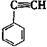 ④CH3-CH=CH-CN,其中可用于合成结构简式为
④CH3-CH=CH-CN,其中可用于合成结构简式为 的高分子材料的正确组合为
的高分子材料的正确组合为
| A.①③④ | B.②③④ | C.①②④ | D.①②③ |
某物质中可能有甲酸、乙酸、甲醇和甲酸乙酯四种物质中的一种或几种。在鉴定时有下列现象:①有银镜反应;②加入新制的Cu(OH)2悬浊液后未发现变澄清;③与含酚酞的NaOH溶液共热,红色逐渐消失。下列结论正确的是
| A.几种物质均存在 | B.有甲酸乙酯和甲酸 |
| C.有甲酸乙酯和甲醇 | D.有甲酸乙酯,可能有甲醇 |
已知乙炔(C2H2)、苯(C6H6)、乙醛(C2H4O)的混合气体中含氧元素的质量分数为8%,则混合气体中碳元素的质量分数为
| A.84% | B.60% | C.91% | D.42% |