某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+和K+。取该溶液100mL,加入过量NaOH溶液并加热,得到0.02mol气体,同时产生红褐色沉淀,将过滤洗涤后的沉淀灼烧得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。下列说法正确的是
| A.该溶液中最多存在4种离子 |
| B.该溶液中不能确定是否存在CO32- |
| C.该溶液中一定存在Cl-、且c(Cl-)≥0.4mol∙L-1 |
| D.该溶液可由KCl、(NH4)2SO4和FeCl3配制而成 |
下述实验能达到预期目的的是
| 编号 |
实验内容 |
实验目的 |
| A |
将SO2通入溴水中 |
验证SO2具有漂白性 |
| B |
在滴有酚酞的Na2CO3溶液中,加入BaC12溶液后红色褪去 |
验证Na2CO3溶液中存在水解平衡 |
| C |
淀粉溶液和稀H2 SO4混合加热,后加新制的Cu(OH)2悬浊液加热至沸腾 SO4混合加热,后加新制的Cu(OH)2悬浊液加热至沸腾 |
检验淀粉水解产物有还原性 |
| D |
将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中 |
检验气体中含有乙烯 |
下列各项内容中,排列顺序正确的是
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3
②相同物质的量浓度的下列溶液中c(NH+4):(NH4)2SO4>NH4)2CO3> NH4Cl
③微粒半径:K+>S2->F
④给出质子的能力:CH3COOH>C2H5OH>H2O
⑤沸点:H2Se> H2S> H2O
NA表示阿伏加德罗常数的值.下列叙述正确的是
| A.18g D2O中含有的中子数为10NA |
| B.64g铜发生氧化还原反应失去的电子数可能为NA |
| C.标准状况下,11.2L己烯中含有的碳原子数为3NA |
| D.25℃时,1mol·L-1醋酸溶液中所含CH3COOH分子总数一定小于NA |
水的电离平衡曲线如图所示。下列说法 中,正确的是
中,正确的是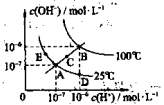
A.图中A、D、E三点处KW间的关系:E处>A处>D处
B.温度不变时,往水中通入适量HCl气体,可以使水的电离
从A点变化到D点
C.温度不变时,在水中加入适量CH3COONa固体,可以使水
的电离从A点变化到C点
D.在B点处,0.5mol·L-1的H2SO4溶液与1mol·L-1的KOH溶液等体积混合,充分反应后,所得溶液的pH=7
下列说法中,不正确的是
| A.短周期元素中,最外层电子数是其电子层数两倍的元素共有3种 |
| B.第三周期元素的离子半径大小比较:Cl->S2+>Na+>Mg2+>Al3+ |
| C.日本福岛核电站释放出的放射性核素131I与132I、133I互为同位素 |
| D.相同条件下,通过测定同浓度的Na2CO3溶液和Na2SO4溶液的pH,可比较C和S的非金属性强弱 |