下列说法不正确的是
| A.原电池外电路中电子由负极流向正极 |
| B.原电池中发生还原反应的电极是正极 |
| C.电解池中发生还原反应的电极是阳极 |
| D.电解池中质量增加的电极是阴极 |
在过滤、蒸馏、萃取和蒸发结晶等物质分离的实验操作中,用不到的仪器是()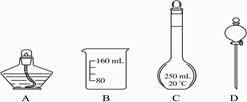
欲萃取碘水中的I2,不能作为萃取剂的是()
| A.酒精 | B.苯 | C.CCl4 | D.汽油 |
下列溶液中微粒的物质的量浓度关系正确的是 ( )
A.室温下,向0.01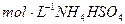 溶液中滴加 溶液中滴加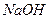 溶液至酸性: 溶液至酸性: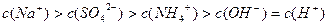  |
B.0.1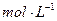 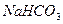 溶液: 溶液: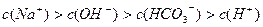  |
C.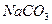 溶液: 溶液: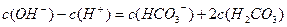  |
D.25℃时,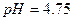 、浓度均为0.1 、浓度均为0.1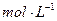 的 的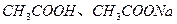 混合溶液: 混合溶液: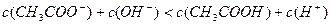 |
下列叙述正确的是 ( )
A.0.1 mol/LC6H5ONa溶液中:c(Na+)>c(C6H5O-)>c(H+)>c(OH-) |
B.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
C.pH=5的CH3COOH溶液和Ph=5的NH4Cl溶液中,c(H+)不相等 |
D.在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降 |
用0.1 mol•.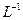 的盐酸滴定0.10 mol•.
的盐酸滴定0.10 mol•.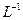 的氨水,滴定过程中不可能出现的结果是( )
的氨水,滴定过程中不可能出现的结果是( )
A.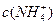 > >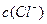 , ,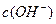 > >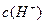 |
B.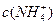 = =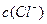 , ,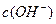 = =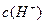 |
C.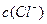 > >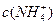 , ,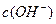 > >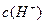 |
D.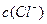 > >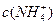 , ,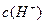 > >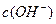 |