以Mg片和Al片为电极,并用导线连接,同时插入NaOH溶液中,下列说法正确的是
A.Mg片作负极,电极反应:Mg-2e-  Mg2+ Mg2+ |
B.Al片作负极,电极反应:Al+4OH- -3e-  AlO2- +2H2 O AlO2- +2H2 O |
| C.电子从Mg电极沿导线流向Al电极 |
| D.Al片上有气泡产生 |
下列取代基或微粒中,碳原子都满足最外层为8电子结构的是
| A.乙基(—CH2CH3) | B.碳化钙 (CaC2) |
| C.碳正离子[(CH3)3C + ] | D.碳烯 ( : CH2 ) |
有机物 的正确命名为
的正确命名为
| A.3,3,4—三甲基已烷 |
| B.3,3—二甲基-4-乙基戊烷 |
| C.2—乙基—3,3-二甲基—4—乙基戊烷 |
| D.2,3,3—三甲基已烷 |
下列有机物分子中有三种不同的氢原子,且氢原子个数之比为3 ∶2 ∶1的是
| A.CH3CHO | B.CH3COOC2H5 | C.CH3COOH | D.CH3CH2OH |
下列各组物质中,全部属于纯净物的是
| A.福尔马林、汽油、食醋 | B.二甲苯、蔗糖、花生油 |
| C.甘油、氯仿、无水酒精 | D.淀粉、天然气、电石气 |
下列化合物中,核磁共振氢谱只出现三组峰且峰面积之比为3:2:2的是 ( )
A.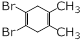 |
B. |
C.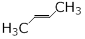 |
D.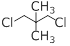 |