镁铝合金5.1 g溶于300mL2mol/L的HCl,在标准状况下放出气体的体积为5.6L。向反应后的溶液中加入足量氨水,产生沉淀的质量为( )
| A.5.1g | B.10.2g | C.13.6g | D.15.3g |
下列装置或操作能达到实验目的的是()
| A.验证反应的热效应 | B.定量测定化学反应速率 |
| C.滴定法测FeSO4 | D.构成铜锌原电池溶液的浓度 |
下列离子或分子组中能大量共存,且满足相应要求的是 ( )
| 选项 |
离子或分子 |
要求 |
| A |
Na+、HCO、Mg2+、SO |
滴加氨水立即有沉淀产生 |
| B |
Fe3+、NO、SO、Cl- |
滴加盐酸立即有气体产生 |
| C |
NH、Al3+、SO、CH3COOH |
滴加NaOH溶液立即有气体产生[ |
| D |
K+、NO、Cl-、HS- |
c(K+)<c(Cl-) |
下列离子方程式与所述事实相符且正确的是()
| A.Ca(HCO3)2溶液中加入少量NaOH溶液: Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O |
| B.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应: 4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
| C.明矾溶液中加入Ba(OH)2溶液至生成的沉淀物质的量最多: Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| D.磁性氧化铁溶于稀硝酸:Fe3O4+8H++NO3-=3Fe3++NO↑+4H2O |
下表所列各组物质中,不能通过一步反应实现如图所示转化的是()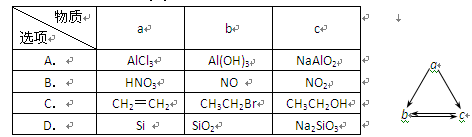
设NA为阿伏伽德罗常数的值。下列叙述正确的是 ( )
| A.20mL 10mol·L-1的浓硝酸或浓硫酸与足量铜加热反应转移电子数均为0.2NA |
| B.0.1mol的白磷(P4)或甲烷中所含的共价键数均为0.4NA |
| C.在精炼铜或电镀铜的过程中,当阴极析出铜32g转移电子数均为NA |
| D.标准状况下,2.24L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA |