用NA表示阿伏加德罗常数,下列叙述不正确的是
| A.标准状况下,22.4LSO3含有的分子数NA |
| B.常温常压下,4.4gCO2的物质的量一定为0.1mol |
| C.标准状况下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
| D.7.8gNa2S和7.8gNa2O2中含有的阴离子数目均为0.1NA |
某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水蒸气都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体。上述说法正确的是()
| A.①②③④ | B.①②⑤⑥ | C.③⑤⑥⑦ | D.①③④⑦ |
阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是()
(1)0.25molNa2O2中含有的阴离子数为0.5×6.02×1023
(2)7.5gSiO2晶体中含有的硅氧键数为0.5×6.02×1023
(3)2.24LCH4中含有的原子数为0.5×6.02×1023
(4)250mL2mol/L的氨水中含有NH3·H2O的分子数为0.5×6.02×1023
(5)1L 1mol·L―1的HAc溶液中含有6.02×1023个氢离子
(6)18g D2O(重水)完全电解,转移6.02×1023个电子
(7)22.4L SO2气体,所含氧原子数为2×6.02×1023
(8)14g乙烯和丙烯的混合物中,含有共用电子对数目为3×6.02×1023
| A.2个 | B.3个 | C.5个 | D.6个 |
某酸性溶液中只有Na+、 、H+、
、H+、 四种离子。则下列描述正确的是( )
四种离子。则下列描述正确的是( )
| A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成 |
| B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
C.加入适量的NaOH,溶液中离子浓度为c( )>c(Na+)>c(OH-)>c(H+) )>c(Na+)>c(OH-)>c(H+) |
D.加入适量氨水,c( )一定大于c(Na+)、c(NH4+)之和 )一定大于c(Na+)、c(NH4+)之和 |
下列离子方程式与所述事实相符且正确的是()
A.漂白粉溶液在空气中失效: +CO2+H2O=HClO+ +CO2+H2O=HClO+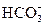 |
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-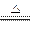 Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
C.向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+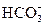 |
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3 +2Fe(OH)3=2 +2Fe(OH)3=2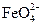 +3 +3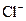 +H2O+4H+ +H2O+4H+ |
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1mol Cu2 (OH)2CO3后恰好恢复到电解前的浓度和pH值(不考虑二氧化碳的溶解)。则电解过程中共转移的电子数为()
| A.0.4mol | B.0.5mol | C.0.6mol | D.0.8mol |