下列事实中,能用勒夏特列原理解释的是
| A.配制FeSO4溶液时,加入一些铁粉 |
| B.500℃左右比室温更有利于合成氨的反应 |
| C.实验室常用排饱和食盐水的方法收集氯气 |
| D.由H2、I2(g)、HI组成的平衡体系,加压后颜色加深 |
已知酸性: >H2CO3>
>H2CO3> ,综合考虑反应物的转化率和原料成本等因素,将
,综合考虑反应物的转化率和原料成本等因素,将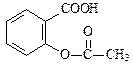 转变为
转变为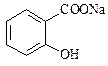 的最佳方法是
的最佳方法是
| A.与稀H2SO4共热后,加入足量NaOH溶液 |
| B.与稀H2SO4共热后,加入足量NaHCO3溶液 |
| C.与足量的NaOH溶液共热后,再通入足量CO2 |
| D.与足量的NaOH溶液共热后,再加入适量H2SO4 |
最近有人用一种称为“超酸”的化合物H (CB11H6Cl6) 和C60反应,使C60获得一个质子,得到一种新型离子化合物[HC60]+[CB11H6Cl6]-.这个反应看起来很陌生,但反应类型上却可以跟下列一个化学反应相似,你认为该反应是
| A.Mg + 2HCl = MgCl2 + H2↑ | B.NaOH + HCl =" NaCl" + H2O |
| C.NH3 + HCl = NH4Cl | D.H2O +CH3COOH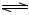 H3O+ +CH3COO- H3O+ +CH3COO- |
下列各组离子在指定条件下,—定能大量共存的是
| A.在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、HCO3-、Na+ |
| B.pH=1的溶液中:Cu2+、Al3+、SO42-、NO3- |
| C.能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH4+、S2-、Br- |
| D.水电离出的c(H+)=10-12mol/L的溶液中:Na+、Mg2+、Cl-、S2- |
下列叙述正确的是
| A.某强碱性溶液中加入足量盐酸产生无色无味且能使澄清的石灰水变浑浊的气体,则该溶液中一定含有大量CO32- |
B.煮沸MgCO3悬浊液,得到M g(OH)2沉淀,说明MgCO3的溶解度小于Mg(OH)2 g(OH)2沉淀,说明MgCO3的溶解度小于Mg(OH)2的溶解度 |
| C.在铁器上电镀铜的实验过程中,电镀液(CuSO4溶液)的pH逐渐升高 |
D.欲制备F(OH)3胶体,向盛有沸水的 烧杯中滴加FeCl3饱和溶液并长时间煮沸 烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
下列说法正确的是