下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠反应的是
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤NaHSO4 ⑥AlCl3 ⑦NaAlO2
| A.①⑤ | B.②③④⑥⑦ | C.①②③④ | D.全部 |
下列烧杯中盛放的都是稀硫酸,在铜电极上能产生气泡的是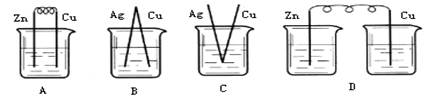
下图是一些常见有机物的转化关系,关于反应①~⑦的说法不正确的是
| A.反应①是加成反应 | B.只有反应②是加聚反应 |
| C.反应④⑤⑥⑦是取代反应 | D.只有⑦是取代反应 |
下列说法正确的是
| A.淀粉、纤维素、油脂、蛋白质都是天然有机高分子化合物 |
| B.实验室只用乙醇和乙酸混合加热就可以制取乙酸乙酯 |
| C.可以用新制的氢氧化铜检验尿液中的葡萄糖 |
| D.乙烯可以与氢气发生加成反应,苯不能与氢气加成 |
以下有关原子结构及元素周期律的叙述正确的是
| A.第IA族元素铯的两种同位素137Cs比133Cs多4个质子 |
| B.同主族元素从上到下,单质的熔点逐渐降低 |
| C.第ⅦA元素从上到下,其氢化物的稳定性逐渐增强 |
| D.同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是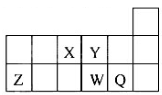
| A.元素X与元素Z的最高正化合价之和的数值等于8 |
| B.原子半径的大小顺序为:rX>rY>rZ>rW>rQ |
| C.离子Y2-和Z 3+的核外电子数和电子层数都不相同 |
| D.元素W的最高价氧化物对应的水化物的酸性比Q的强 |