铜镁合金9.2g完全溶于浓硝酸中,反应中硝酸钡还原只产生10304mL(标准状况下)NO2气体。向反应后的溶液中加足量NaOH溶液,生成沉淀的质量为( )
| A.16.51g | B.23.82g | C.24.84g | D.17.02g |
硫酸亚铁是一种重要的化工原料,可以制备多种物质。有关下列制备方法错误的是
| A.制备碱式硫酸铁利用了过氧化氢的氧化性 |
| B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行 |
| C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化 |
| D.制备(NH4)2Fe(SO4)2利用了它的溶解度比FeSO4的溶解度大这一性质 |
把锌片和铁片放在盛有稀稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中(如图所示平面图),经过一段时间后,下列说法中正确的是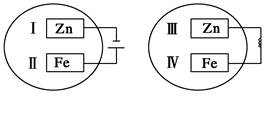
| A.Ⅰ附近溶液pH降低 | B.Ⅱ附近很快出现蓝色沉淀 |
| C.Ⅲ附近产生黄绿色气体 | D.Ⅳ附近很快生成铁锈 |
下列说法中正确的有几项
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.5mol/L的NaOH溶液,需要用托盘天平称量氢氧化钠固体9.6g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeCl2、H2SiO3都不直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的氨水等体积混合后,所得溶液中溶质的质量分数大于15%
⑦干燥的Cl2和氯水均能使鲜花褪色
⑧中和热测定实验中需要用到的玻璃仪器只有烧杯、温度计和环形玻璃搅拌棒三种
⑨纯银器在空气中久置变黑是因为发生了化学腐蚀
| A.3项 | B.4项 | C.5项 | D.6项 |
下面是几种常见的化学电源示意图,有关说法不正确的是
| A.上述电池分别属于一次电池、二次电池和燃料电池 |
| B.干电池在长时间使用后,锌筒被破坏 |
| C.铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g |
| D.氢氧燃料电池是一种具有应用前景的绿色电源 |
1L某溶液中含有的离子如下表:
| 离子 |
Cu2+ |
Al3+ |
NO3- |
Cl- |
| 物质的量浓度(mol/L) |
1 |
1 |
a |
1 |
用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积的变化及电解产物可能存在的溶解现象),下列说法正确的是
A.电解后溶液pH=0 B.a=3
C.阳极生成1.5mol Cl2 D.阴极析出的金属是铜与铝