【化学-选修3:物质结构与性质】
A、B、C、D、E五种常见元素的核电荷数依次增大。A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物,E的基态3d轨道上有2个电子。请回答下列问题:
(1)E的基态原子价层电子排布式为________________。
(2)AB2分子中,A的杂化类型为________________;在元素周期表中A、B及与两者紧邻的元素的第一电离能由大到小的顺序为(用元素符号表示)__________________。
(3)B的氢化物与D的氢化物的沸点较高的是____________(用化学式表示),原因是______________。
(4)AB2形成的晶体的熔点____________(填“高于”“低于”或“无法判断”)CD形成的晶体的熔点,原因是___________________。
(5)E与B形成的一种橙红色晶体晶胞结构如图所示,其化学式为____________(用元素符号表示)。ED4是制取航天航空工业材料的重要原料。取上述橙红色晶体,放在电炉中,通入D2和A的单质后高温加热,可制得ED4,同时产生一种造成温室效应的气体,写出反应的化学方程式:_________________________。
(6)由C、D两元素形成的化合物组成的晶体中,晶体结构图以及晶胞的剖面图如下图所示,若晶胞边长是acm,则该晶体的密度为____________g/cm3.(已知阿伏加德罗常数为NA)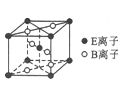

(14分)阿立哌唑(A)是一种新的抗精神分裂症药物,可由化合物B、C、D在有机溶剂中通过以下两条路线合成得到。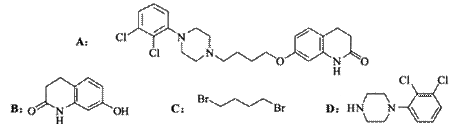
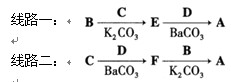
(1)E的结构简式为。
(2)由C、D生成化合物F的反应类型是。
(3)合成F时还可能生成一种相对分子质量为285的副产物G,G的结构简式为。
(4)H属于 氨基酸,与B的水解产物互为同分异构体。H能与
氨基酸,与B的水解产物互为同分异构体。H能与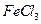 溶液发生显色反应,且苯环上的一氯代物只有2种。写出两种满足上述条件的H的结构简式:。
溶液发生显色反应,且苯环上的一氯代物只有2种。写出两种满足上述条件的H的结构简式:。
( 5)已知:
5)已知: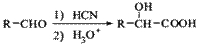 ,写出由C制备化合物
,写出由C制备化合物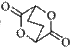 的合成路
的合成路
线流程图(无机试剂任选)。合成路线流程图示例如下: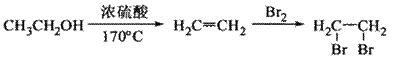
正极材料为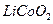 的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
(1)橄榄石型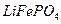 是一种潜在的锂离子电池正极材料,它可以通过
是一种潜在的锂离子电池正极材料,它可以通过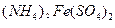 、
、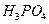 与
与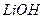 溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
①共沉淀反应投料时,不将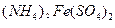 和
和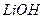 溶液直接混合的原因是。
溶液直接混合的原因是。
②共沉淀反应的化学方程式为。
③高温成型前,常向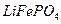 中加入少量活性炭黑,其作用除了可以改善成型后的
中加入少量活性炭黑,其作用除了可以改善成型后的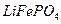 的导电性能外,还能。
的导电性能外,还能。
(2)废旧锂离子电池的正极材料试样(主要含有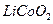 及少量AI、Fe等)可通过下列实验方法回收钴、锂。
及少量AI、Fe等)可通过下列实验方法回收钴、锂。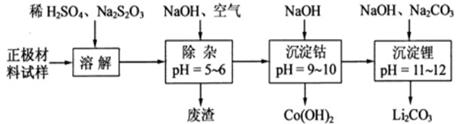
①在上述溶解过程中,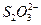 被氧化成
被氧化成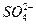 ,
,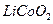 在溶解过程中反应的化学方程式为。
在溶解过程中反应的化学方程式为。
②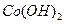 在空气中加热时,固体残留率随温度的变化,如下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为。(填化学式);在350~400℃范围内,剩余固体的成分为。(填化学式)。
在空气中加热时,固体残留率随温度的变化,如下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为。(填化学式);在350~400℃范围内,剩余固体的成分为。(填化学式)。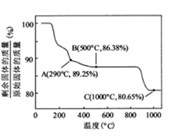
下表列出了3种燃煤烟气脱硫方法的原理。
(1)方法Ⅰ中氨水吸收燃煤烟气中 的化学反应为:
的化学反应为: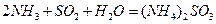

能提高燃煤烟气中 去除率的措施有__________(填字母)。
去除率的措施有__________(填字母)。
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D . 通入空气使
. 通入空气使 转化为
转化为
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的 ,原因是▲(用离子方程式表示)。
,原因是▲(用离子方程式表示)。
(2)方法Ⅱ重要发生了下列反应:
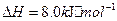






 与
与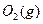 反应生成
反应生成 的热化学方程式为
的热化学方程式为 。
。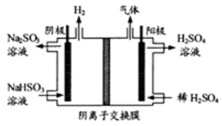
(3)方法Ⅲ中用惰性电极电解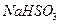 溶液的装置如上图所示。阳极区放出气体的成分为。(填化学式)
溶液的装置如上图所示。阳极区放出气体的成分为。(填化学式)
以水氯镁石(主要成分为 )为原料生产碱式碳酸镁的主要流程如下:
)为原料生产碱式碳酸镁的主要流程如下:
(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的 ,若溶液中
,若溶液中 ,则溶液中
,则溶液中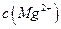 = 。
= 。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 。
。
(3)高温煅烧碱式碳酸镁得到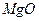 。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下
。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下 0.896L,通过计算确定碱式碳酸镁的化学式。
0.896L,通过计算确定碱式碳酸镁的化学式。
(4)若热水解不完全,所得碱式碳酸镁中将混有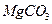 ,则产品中镁的质量分数▲ (填 “升高”、“降低”或“不变”)。
,则产品中镁的质量分数▲ (填 “升高”、“降低”或“不变”)。
钡盐行业生产中排出大量的钡泥[主要含有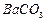 、
、 、
、 、
、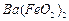 等。某主要生产
等。某主要生产 、
、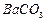 、
、 的化工厂利用钡泥制取
的化工厂利用钡泥制取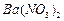 ,其部分工艺流程如下:
,其部分工艺流程如下: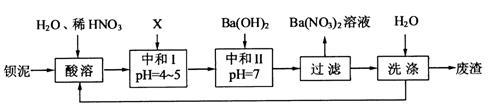
(1)酸溶后溶液中 ,
,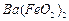 与
与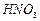 的反应化学方程式为 。
的反应化学方程式为 。
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,
原因是 、 。
(3)该厂结合本厂实际,选用的X为 (填化学式);中和Ⅰ使溶液中 (填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略)。
(4)上述流程中洗涤的目的是 。