在我们的日常生活中出现了“加碘食盐”“铁强化酱油”“高钙牛奶”“含氟牙膏”等商品。这里的碘、铁、钙、氟应理解为
| A.元素 | B.单质 | C.分子 | D.氧化物 |
可用于判断碳酸氢钠粉末中混有碳酸钠的实验方法是()
| A.加热时有无色气体放出 |
| B.滴加盐酸时有气泡放出 |
| C.溶于水后滴加澄清石灰水,有白色沉淀生成 |
D.溶于水后滴加BaCl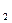 稀溶液,有白色沉淀生成 稀溶液,有白色沉淀生成 |
下列物质既能与盐酸作用,又能与澄清石灰水作用的是()
| A.NaOH | B.NaNO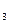 |
C.Na SO 4 SO 4 |
D.NaHCO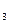 |
向0.1 mol·L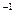 NaOH溶液中通入过量CO
NaOH溶液中通入过量CO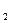 后,溶液中存在的主要离子是()
后,溶液中存在的主要离子是()
A.Na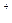 、CO 、CO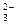 |
B.Na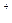 、HCO 、HCO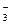 |
C.HCO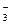 、CO 、CO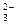 |
D.Na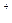 、OH 、OH |
下列氢氧化物中碱性最强的是()
| A.KOH | B.NaOH | C.LiOH | D.CsOH |
下列实验操作或说法,正确的是()
| A.向盛水的烧杯中投入一大块钠,这样现象更明显 |
B.钠也可以保存在CCl 中 中 |
| C.将一小块钠放在石棉网上加热,观察现象 |
| D.钠很软,可用手掰开来观察它的颜色 |