25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是
A.2H2(g)+O2(g) ="=" 2H2O(1)△H= ―285.8kJ/mol |
| B.2H2(g)+ O2(g) ="=" 2H2O(1)△H= +571.6 kJ/mol |
| C.2H2(g)+O2(g) ="=" 2H2O(g)△H= ―571.6 kJ/mol |
D.H2(g)+ O2(g) ="=" H2O(1)△H= ―285.8kJ/mol O2(g) ="=" H2O(1)△H= ―285.8kJ/mol |
17.阿波罗宇宙飞船以N2H4(联氨)和N2O4为动力源,反应温度达27000C,反应化学方程式为 2N2H4+N2O4= 3N2+4H2 O,下列关于该反应的叙述正确的是:
O,下列关于该反应的叙述正确的是:
C.N2H4是还原剂 D.N2是氧化产物,不是还原产物
向体积为Va的0.05 mol·L-1 CH3COOH溶液中加入体积为Vb的0.05 mol·L-1 KOH溶液,下列关系错误的是( )
| A.Va>Vb时:c(CH3COOH)+c(CH3COO-)>c(K+) |
| B.Va=Vb时:c(CH3COOH)+c(H+)=c(OH-) |
| C.Va<Vb时:c(CH3COO-)>c(K+)>c(OH-)>c(H+) |
D.Va与Vb任意比时:c(K+)+c(H+)=c(OH-) +c(CH3COO-) +c(CH3COO-) |
下列各组热化学方程式中,△H1>△H2的是()
①C(s)+O2(g)===CO2(g)△H1 C(s)+1/2O2(g)="==CO(g)" △H2
②S(s)+O2(g)===SO2(g)△H1 S(g)+O2(g)===SO2(g)△H2
③H2(g)+1/2O2(g)===H2O(l)△H1 2H2(g)+O2(g)===2H2O(l)△H2
④CaCO3(s)===CaO(s)+CO2(g)△H1 CaO(s)+H2O(l)===Ca(OH)2(s)△H2
| A.① | B.④ | C.②③④ | D.①②③ |
下列液体均处于25℃,有关叙述正确的是()
| A.某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
| B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
| C.在1 mol/L的氨水中,改变外界条件使c(NH4+)增大,则溶液的pH一定增大 |
D.NaHCO3溶液中:c(Na+)=2c(CO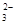 )+c(HCO )+c(HCO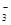 )+c(H2CO3) )+c(H2CO3) |
等 量的苛性钠溶液分别用pH=2和pH=3的醋酸溶液中和,设消耗的醋酸溶液的体积依次为Va、Vb,则两者的关系正确的为()
量的苛性钠溶液分别用pH=2和pH=3的醋酸溶液中和,设消耗的醋酸溶液的体积依次为Va、Vb,则两者的关系正确的为()
| A.Va >10 Vb | B.Vb =10Va | C.Vb<10 Va | D.Vb>10 Va |