黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)==K2S(s)+N2(g)+3CO2(g)ΔH=xkJ·mol-1
已知碳的燃烧热ΔH1=akJ·mol-1
S(s)+2K(s)==K2S(s)ΔH2=bkJ·mol‾1
2K(s)+N2(g)+3O2(g)==2KNO3(s)ΔH3=ckJ·mol‾1,则x为
| A.3a+b-c | B.c+3a-b | C.a+b-c | D.c+a-b |
下列说法正确的是
A.氢气的燃烧热为△H=-285.5kJ•mol-1,则电解水的热化学方程式为2H2O(l)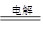 2H2(g)+O2(g) △H=+285.5k•Jmol-1 2H2(g)+O2(g) △H=+285.5k•Jmol-1 |
| B.反应SO2(g)+2H2S(g)=3S(s)+2H2O(l)在常温下能自发进行,则该反应的△H<0 |
| C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) +3H2(g)═2NH3(g)△H=-38.6k•Jmol-1 |
| D.由C(石墨,s)=C(金刚石,s) △H="+1.90" k•Jmol-1可知,金刚石比石墨稳定 |
固体A的化学式为NH5,它的所有原子的最外层均满足2个或8个电子的稳定结构。则下列有关说法中错误的是
| A.1mol NH5中含有5NA个N-H键(NA表示阿伏加德罗常数的值) |
| B.NH5中既有共价键又有离子键 |
C.NH5的电子式为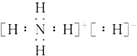 |
| D.它与水反应的化学方程式为NH5+H2O═NH3•H2O+H2↑ |
下列与NaHSO3溶液有关的离子方程式书写错误的是
| A.NaHSO3溶液与FeCl3反应:HSO3-+2 Fe3++H2O=SO42-+2Fe2++3H+ |
| B.NaHSO3溶液和足量Ca(OH)2溶液反应:Ca2++OH-+HSO3-=CaSO3↓+H2O |
| C.NaHSO3溶液和稀HNO3反应:HSO3-+H+=SO2↑+H2O |
| D.NaHSO3溶液和NaAlO2溶液反应:HSO3-+ AlO2-+H2O=SO32-+Al(OH)3↓ |
下列离子或分子能够在指定的分散系中大量共存的是
| A.与铝反应生成大量氢气的溶液中:Mg2+、K+、HCO3-、NO3- |
| B.0.1mol/L的NaNO3溶液中:K+、I-、Cl-、SO42- |
| C.铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- |
| D.空气中:SO2、NO、N2、NH3 |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,3.4gH2O2含有极性键的数目为0.2NA |
| B.1molCl2和足量氢氧化钠溶液充分反应,转移电子数目为2NA |
| C.电解精炼铜时,若转移了NA个电子,则阳极质量减小32g |
| D.标况下,11.2LSO3所含的分子数目为0.5NA |