下列关于杂化轨道的叙述不正确的是
| A.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构 |
| B.杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对 |
| C.杂化前后的轨道数不变,但轨道的形状发生了改变 |
| D.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180° |
化学与环境密切相关,下列有关说法正确的是
| A.酸雨是PH小于7的雨水 |
| B.CO2、NO2或SO2都会导致酸雨的形成 |
| C.CO2属于大气污染物 |
| D.大气中CO2含量的增加会导致温室效应加剧 |
请将正确的序号填入空白处,下列物质中:
属于酸性氧化物的是属于碱性氧化物的是
属于电解质的是
①NaHSO4②CO2③NaCl溶液④NH4Cl⑤乙醇
⑥SO2⑦Na2O2⑧CaO⑨蔗糖⑩熔融的NaOH
A、B、C、X均为中学化学常见物质,一定条件下它们有如图转化关系(其他产物已略去),下列说法错误的是( )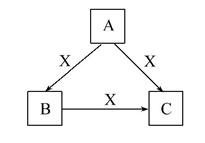
A.若X为Cl2,则C可能为FeCl3
B.若X为KOH溶液,则A可能为AlCl3
C.若X为O2,则A可能为硫化氢
D.若A、B、C均为焰色反应呈黄色的化合物,则X可能为CO2
下列做法不正确的是( )。
| A.易燃试剂与强氧化性试剂分开放置并远离火源 |
| B.用湿润的红色石蕊试纸检验氨气 |
| C.在50 mL量筒中配制0.1000 mol·L-1碳酸钠溶液 |
| D.金属钠着火时,用细沙覆盖灭火 |
关于3Cl2 + 6KOH  KClO3 + 5KCl + 3H2O反应,以下说法正确的是 ()
KClO3 + 5KCl + 3H2O反应,以下说法正确的是 ()
| A.Cl2是氧化剂,KOH是还原剂 |
| B.被氧化的氯元素的质量为被还原的氯元素质量的5倍 |
| C.3mol氯气参加反应转移10mol电子 |
| D.KOH既不是氧化剂,又不是还原剂 |