液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料 的电池装置如图所示,该电池以空气中的氧气为氧化剂,以 KOH 溶液为电解质溶液.下列关于该电池的叙述错误的是( )
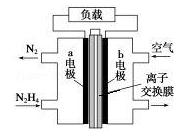
| A.b 极发生还原反应 | |
B.a 极的反应式为 N2H4﹣4e﹣═N2↑+4H+ |
C.放电时,电流从 b 极经过负载流向 a 极 |
| D.其中的离子交换膜需选用阴离子交换膜 |
一定条件下,中学化学常见物质甲、乙存在转化关系,则乙可能是( )
| A.Al(OH)3 | B.H2SiO3 | C.FeCl2 | D.CH3C1 |
下表中根据实验操作和现象所得出的结论正确的是()
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
用激光笔照射鸡蛋白的水溶液 |
有丁达尔效应 |
鸡蛋白粒子直径介于1nm~100nm |
| B |
向某氯化亚铁溶液中,加入Na2O2粉末 |
出现红褐色沉淀 |
说明原氯化亚铁已被氧化而变质 |
| C |
将气体X通入酸化的BaCl2溶液 |
产生白色沉淀 |
X可能是CO2 |
| D |
湿润的KI淀粉试纸靠近气体Y |
试纸变蓝 |
Y一定是Cl2 |
化学与社会、生活、环境保护密切相关。下列现象或事实与解释一致的是( )
| 编号 |
现象与事实 |
解释 |
| A |
用热的纯碱溶液洗涤油污 |
纯碱可以增强油污的挥发性 |
| B |
在农田施肥时,草木灰(主要成分 K2CO3)不能与NH4Cl混合使用 |
NH4+水解生成的HCI与CO32-反 应生成大量CO2 |
| C |
漂白粉在空气中放置时间过久而 变质 |
漂白粉中CaCl2与空气中CO2 反应生成CaCO3,不溶于水 |
| D |
利用FeCl3溶液腐蚀铜箔,制造印刷线路板 |
2FeCl3+Cu2FeCl2+CuCl2 |
某同学通过实验探究铝及其化合物的性质,操作正确且能达到目的的是()
| A.向氯化铝溶液中滴加过量氨水,最终得到澄清溶液 |
| B.等质量的铝粉分别与足量的盐酸和氢氧化钠溶液反应,可制得等质量的氢气 |
| C.常温下,铝与浓硝酸反应可制得大量的NO2 |
| D.AICl3溶液加热蒸干得到无水氯化铝晶体 |
N2O俗称“笑气”,医疗上曾用作可吸入性麻醉剂,下列反应能产生N2O:
3CO+2NO2 3CO2 +N2O。下列说法一定正确的是()
| A.上述反应,每生成lmolN20,消耗67.2LCO |
| B.等物质的量的N2O和CO2含有相等的电子数 |
| C.N2O只有氧化性,无还原性 |
| D.上述反应中,N2O是氧化产物 |