某班同学用氢氧化钠溶液和稀盐酸进行中和反应实验。
(1)甲同学在烧杯中加入约15mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈
色。接着用滴管滴入一定量的稀盐酸,再用玻璃棒搅拌,发现溶液变为无色,反应的化学方程式为 。
(2)甲、乙、丙同学对反应后溶液中的溶质成分进行探究。
【猜想与假设】反应后溶液中的溶质是什么?
猜想一:只有NaCl
猜想二:
猜想三:有NaCl和NaOH
上猜想中,直接可以排除的是 ,理由 。
【实验探究】
为了验证另外两种猜想,甲、乙、丙同学设计如下实验方案:
实验操作 |
实验现象 |
实验结论 |
|
甲同学方案 |
取少量反应后的溶液于试管中向试管中滴加AgNO 3溶液 |
有白色沉淀产生 |
猜想一成立 |
乙同学方案 |
取少量反应后的溶液于试管 中,向试管中加入 |
有气泡产生 |
猜想二成立 |
丙同学方案 |
取少量反应后的溶液于试管中,向试管中加入生锈的铁钉 |
|
猜想二成立 |
丙同学认为甲同学方案不合理,你认为理由是 。
【反思交流】
实验结束后,废液处理方法正确的是 (填序号)。
A.倒入下水道 B.倒入废液缸 C.带出实验室
(9分)实验室有一瓶保存不当的试剂(如下图所示),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是初中化学常用的试剂。小华等几位同学很感兴趣,决定对其成分进行探究。
【提出问题】这瓶试剂溶质是什么?
【交流研讨】根据受损标签的情况判断,这瓶试剂不可能是(填字母序号)。
A.酸B.碱C.盐
【查阅资料】①初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
②Na2CO3、NaHCO3溶液都呈碱性。NaCl溶液呈中性。
③室温下(20℃)时,4种物质的溶解度的数据如下。
| 物质 |
NaCl |
NaOH |
Na2CO3 |
NaHCO3 |
| 溶解度/g |
36 |
109 |
215 |
9.6 |
【得出结论】小华根据试剂瓶上标注和上表溶解度数据判断,这瓶试剂不可能是。
【猜想与实验】①可能是溶液;
②可能是NaOH溶液;
③可能是NaCl溶液。
(1)小亮用洁净的玻璃棒蘸取该溶液,滴到干燥的pH试纸上,测得pH=11,他判断该溶液不可能是。
(2)小强为了确定该溶液的成分,进行了如下实验。
| 操作步骤 |
实验现象 |
结论 |
| 步骤一:取样品于试管中,滴加足量 |
产生大量的气泡 |
猜想①正确。 |
| 步骤二:把产生的气体,通入 |
【质疑】小华则不同意小强的观点,认为溶液中有Na2CO3还可能有NaOH。请你帮助他完成以下探究方案:
| 探究步骤 |
预计现象 |
结论 |
| 步骤一:取样品于试管中,向其中滴加足量的溶液并过滤 |
产生白色沉淀 |
溶液中既含Na2CO3,又含有NaOH |
| 步骤二:向上述滤液中滴加酚酞试液 |
酚酞试液变色 |
某化学兴趣小组展示了他们设计的“火龙生字”创新实验,用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体如图所示。用带火星的木条接触硝酸钾晶体,立即有火花出现,并缓慢地沿着字的笔迹蔓延,最后呈现出“火”字的黑色痕迹(见下图)。现场的同学对此产生了浓厚的兴趣,随后进行了如下研究:
【提出问题】为什么附有硝酸钾的白纸更容易燃烧?
【查阅资料】硝酸钾不可燃烧,但受热易分解,生成亚硝酸钾(KNO2)和一种常见的气体单质。
【猜想与假设】对于产生的是什么气体,四位同学有如下猜测:
甲:二氧化氮; 乙:氮气; 丙:氧气;丁:氢气;
丙同学首先排除了二氧化氮,理由是;同学认为也不可能是氢气,他的理由是 。
【进行实验】四位同学设计了实验对丙同学的猜想进行了验证,他们的操作方法是:,观察到的现象是,说明丙同学的猜想正确,硝酸钾分解的化学方程式是。
【解释与结论】白纸上写过字的地方更容易燃烧的原因是。
【反思与评价】为什么要用“硝酸钾的热饱和溶液”书写文字?
已知硝酸钾在不同温度时的溶解度如下表:
你对上述问题的解释是。
在购买和使用化肥时,要了解化肥的性质,以便合理施用。为了给爸爸做技术指导,小红
利用自己掌握的知识对碳酸钾(K2CO3)、硫酸铵[(NH4)2SO4]两种化肥的相关性质做了以下
探究。
【实验探究】
| 探 究 过 程 |
实 验 现 象 |
结论及化学方程式 |
|
| K2CO3 |
(NH4)2SO4 |
||
| (1)配制碳酸钾、硫酸铵溶液。分别取碳酸钾和硫酸铵固体,加足量水搅拌。 |
得到澄清溶液,温度无明显变化 |
得到澄清溶液,温度明显降低 |
都易溶于水,硫酸铵溶于水时吸收的热量大于放出的热量。 |
| (2)猜想与假设。 碳酸钾、硫酸铵溶液的酸碱性都可能有种情况。 分别取少量两种溶液于两只试管中,滴加紫色石蕊试液。 |
变蓝 |
变红 |
说明碳酸钾溶液显碱性; 说明硫酸铵溶液显 性。 |
| (3)与盐酸反应。 分别取少量两种溶液于两只试管中,加入稀盐酸。 |
无明显现象 |
碳酸钾能与酸反应。 |
|
| (4)与氢氧化钠溶液反应。 分别取少量两种溶液于两只试管中,加入氢氧化钠溶液,微热。 |
无明显现象 |
有气泡产生且有刺激性气味 |
硫酸铵能与碱反应。写出相关的化学方程式: |
【结论与应用】碳酸钾与硫酸铵(填“能”或“不能”)混用,说明原因。
某实验小组取用生石灰时,发现装满生石灰的塑料试剂瓶已经膨胀破裂,于是小组中的几位同学对其中的成分进行了探究。
【提出猜想】小丹认为含有CaO、Ca(OH)2、CaCO3;
小凯认为含有CaO、Ca(OH)2;
小欣认为含有Ca(OH)2、CaCO3。
【设计实验】
| 实验操作 |
实验现象 |
结论 |
|
| 步骤一 |
取试样于试管中加水振荡 |
液体浑浊,用手摸试管外壁,感觉不发热 |
_________________ |
| 步骤二 |
向步骤一的试管中滴加无色酚酞溶液 |
溶液变红色 |
_________________ |
| 步骤三 |
____________________________ |
试管内有气泡生成 |
一定含有CaCO3 |
【得出结论】(1)通过以上探究可知_________同学的猜想正确,
请写出使CaO变质的化学方程式。
【注意:若答对第(2)小题奖励4分,化学试卷总分不超过60分。】
【拓展】(2)如果生石灰已全部变质为碳酸钙,请你设计实验加以证明(写出必要的步骤、现象和结论)。_________________________________________________________________
_________________________________________________________________
_________________________________________________________________
某研究性学习小组设计了测定纯碱(Na2CO3)样品(只含NaCl杂质)中Na2CO3质量分数的实验方案.请回答下列问题:
小资料:碱石灰的主要成分是氢氧化钠和氧化钙的混合物
(1)气体法。
【原理思路】利用Na2CO3与稀硫酸反应产生CO2,通过测量丙装置实验前后的质量得出CO2质量,从而计算碳酸钠的质量分数。(不考虑原装置内空气的影响)
【实验分析】小科同学根据以上思路,设计了如图实验装置。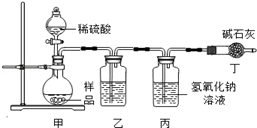
①实验装置乙中盛放的试剂为,其作用是;
装置丁中碱石灰的作用是。(填字母)
A.吸收Na2CO3与稀硫酸反应产生CO2
B.防止外界空气中二氧化碳进入丙中
C.干燥二氧化碳
②实验中如果滴加稀硫酸的速度过快,会导致测得样品中碳酸钠的质量分数(填写“偏高”、“偏低”或“不变”).
③小明同学认为小科的方案存在问题,不考虑原装置内空气的影响,即使操作规范,但由于生成的CO2在装置中残留,也会造成测得结果(填写“偏高”、“偏低”或“不变”),应该将装置甲中双孔橡胶塞换成三孔橡胶塞,并增加下图装置,实验结束后缓缓通入一段时间空气,目的是,其中图中NaOH溶液的作用是。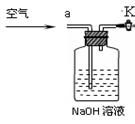
(2)沉淀法.
【实验原理】利用碳酸根离子与钙离子结合生成沉淀,通过沉淀的质量而得出碳酸钠的质量分数。
【实验步骤】①用托盘天平称取样品11.0g放入烧杯中,加水使其完全溶解;
②加入过量的CaCl2溶液充分反应。证明CaCl2过量(即让样品中Na2CO3完全反应)的方法是:静置,向上层清液中滴加溶液,如果没有白色沉淀生成,证明CaCl2过量;
③过滤、洗涤、干燥、称量沉淀的质量为10.0g,由于沉淀表面粘附滤液,不经洗涤就烘干,称量沉淀的质量将会(填写“偏高”、“偏低”或“不变”)。
④通过以上提供的数据计算出样品中碳酸钠的质量分数。(写出计算过程,结果保留至0.1%,共3分,只写出化学方程式给1分)