一些金属易生锈,某小组同学设计如下实验,对金属锈蚀进行探究.
【实验一】取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验.
实验图示 |
|
|
|
|
|
生锈时间 |
8min |
较长时间不生锈 |
5min |
3min |
1min |
(1)通过上述实验可知,温度越高铁钉生锈速率越 (填“慢”或“快”);在 (填“酸性”、“碱性”或“中性”)环境中铁钉生锈速率较快.
【实验二】为探究铁锈的成分,用图1所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全).
【查阅资料】无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收CO2.
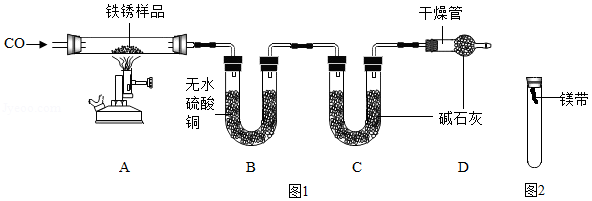
(2)请指出图1所示实验装置的一个明显缺陷: .
(3)加热前,先通入CO一段时间,目的是 .
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝, 由此推知铁锈中一定含有 元素,从而推断出空气中的 参加了铁生锈反应.
【实验记录】
铁锈样品的质量/g |
装置B的质量/g |
装置C的质量/g |
|
反应前 |
23.2 |
232.4 |
198.2 |
反应后 |
/ |
239.6 |
211.4 |
(5)根据上表数据推算,可确定铁锈的成分,用FexOy•nH2O表示,则n= ;若缺少D装置,x:y的值 (填“偏大”、“偏小”或“无影响”).
(6)欲通过实验探究镁带在空气中锈蚀的条件,用图2所示装置,试管内可选用的物质如下:
①O2②水③CO2④O2和CO2⑤CO2和水⑥O2和水⑦O2、CO2和水
至少需要选用 (填数字序号),才能达到探究镁带锈蚀的条件.
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁[Mg3(OH)2(CO3)2]的化学方程式 .
有一包固体,可能含有NaCl、NaOH、Na 2CO 3、Na 2SO 4、MgCl 2中的一种或几种。为确定其组成,取少量固体加足量水溶解得到无色溶液M,进行如图实验。

试推断:
(1)白色沉淀B是 (填化学式)。
(2)原固体中一定含有的物质是 。
(3)无色滤液2中一定含有的阳离子是 (填离子符号)。
(4)通过上述实验可知还有一种物质不能确定是否存在,为进一步确定,应采用的方法是 方法一:______;
方法二:______。
根据如图回答问题:

(1)实验室用高锰酸钾制取并收集较纯净的氧气,应选用的装置是 (填字母)。向气体发生装置内加入药品前应进行的操作是 。
(2)实验室用石灰石和稀盐酸反应制取二氧化碳时,可选用发生装置A或G,G与A相比较,其优点是 ;若用F 装置收集二氧化碳,检验二氧化碳已收集满的方法是 。如果要证明制取二氧化碳实验后的废液呈酸性,可选用的试剂是 (填字母)。
a.紫色石蕊溶液 b.石灰石 c.氢氧化钠溶液 d.硝酸银溶液 e.铜
化学是一门以实验为基础的科学。根据下图所示装置回答有关问题:

(1)仪器①的名称是 。
(2)李丽同学设计了实验室制取并收集二氧化碳的装置(如图C所示),装置中出现了一处错误,你的纠正方法是 ,该装置的发生装置具有的优点是 ,锥形瓶中发生反应的化学方程式为 。
(3)实验室利用图A所示装置制取氧气的化学方程式为 。
(4)实验室可以用加热氯化铵和熟石灰固体混合物的方法制取氨气。 已知氨气是一种无色有刺激性气味的气体,密度比空气小,极易溶于水。为了制取并收集一瓶干燥的氨气,且减少对空气的污染,在上述装置中选出最佳的实验装置组合是 (填字母编号)。
实验室里现有硫酸钾、二氧化锰、稀硫酸、石灰石、稀盐酸以及下列仪器

(1)写出下列仪器的名称:② 、④ 。
(2)使用仪器①③④⑤⑦⑩,可以做制取 的实验,反应的化学方程式为 ,此反应属于 (填"化合""分解""置换""复分解")反应;收集完气体后,发现气体不纯,可能的原因是 (写出一条即可)。
(3)制取并收集一瓶二氧化碳气体,除使用仪器②⑥,还需使用如图仪器中的 (填序号)。反应的化学方程式为 ,收集二氧化碳时,证明是否集满的方法是 。
如图是实验室制取气体的有关装置,结合装置图回答下列问题:

(1)结合A﹣G装置图,归纳实验室制取氧气和二氧化碳的共同点 (选填字母)。
a.需要加热 b.需用催化剂 c.没有气体参加反应 d.生成气体只有一种 e.能用B作发生装置
(2)写出用高锰酸钾制取氧气的化学方程式 。小强将A和F连接,用高锰酸钾制取氧气时,发现F装置中的水变成紫色,其原因是 。
(3)若要检验G中氧气是否收集满,需要带火星的木条放置于 处(选填'a'或'b')。
(4)与装置B比较,指出C装置的一个突出优点 。