已知NaHCO 3受热后会分解生成Na 2CO 3,小红同学把84g的NaHCO 3加热一段时间后,称得剩余固体(不含水分)。质量为68.5g。提示:(2NaHCO 3  Na 2CO 3+H 2O+CO 2↑)
Na 2CO 3+H 2O+CO 2↑)
请回答问题:
(1)CO 2由 元素组成,水分子中氢原子与氧原子的个数比为 ;
(2)CO 2的相对分子质量是 ;
(3)此时生成的二氧化碳质量是 ;
(4)计算此时剩余固体中碳元素的质量分数。(写出计算过程,结果精确到0.1%)
20℃时,硝酸钾的溶解度为31.6g,将20g硝酸钾投进50g水中,充分搅拌,制成20℃时的溶液,求该溶液中溶质的质量分数.
把10g铁和铜的混合物放到盛有足量盐酸的烧杯中,充分反应后,烧杯中物质的总质量比反应前(铁、铜混合物和盐酸)减少了0.2g,求原混合物中铜的质量分数.
为测定某赤铁矿石中氧化铁的质量分数,小龙和他的同学用足量的纯净的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,该溶液总质量与反应时间的变化关系如图所示.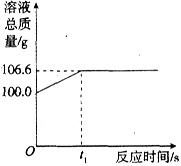
(1)上述反应产生二氧化碳的质量为________g.
(2)计算该赤铁矿石中氧化铁的质量分数.
(3)若上述反应后剩余固体的质量为mg,写出计算该赤铁矿石中氧化铁质量分数的表达式:________________________(用m表示).
某厂排放的废水中含有碳酸钠,易造成环境污染.化学兴趣小组为该厂设计废水处理和利用的方案,进行了如下实验:取过滤后的水样200g,逐滴加入稀盐酸至恰好不再产生气体为止,反应过程中生成气体与所加稀盐酸的质量关系如图所示.回答下列问题(不考虑水样中杂质的影响):
(1)反应生成CO2气体的质量是________g.
(2)反应后生成氯化钠的质量是多少?(写出计算过程)
(3)农业上常用10%~20%的氯化钠溶液来选种.请通过列式计算判断:上述实验恰好完全反应后所得溶液能否直接用于农业上选种?
已知:Na2CO3受热不易分解,2NaHCO4 Na2CO3+CO2↑+H2O.某纯碱样品中混有少量的碳酸氢钠,为了测定样品的纯度,华雪同学做了如下实验:准确称取样品10.0g放入试管中,加热充分反应至无气体放出,共产生CO2气体224mL(该条件下气体的密度为1.964g/L).请回答下列问题:
Na2CO3+CO2↑+H2O.某纯碱样品中混有少量的碳酸氢钠,为了测定样品的纯度,华雪同学做了如下实验:准确称取样品10.0g放入试管中,加热充分反应至无气体放出,共产生CO2气体224mL(该条件下气体的密度为1.964g/L).请回答下列问题:
(1)生成CO2的质量为________g(精确到0.01g).
(2)纯碱样品中的Na2CO3的质量分数是多少?(要求写出计算过程,结果精确到0.1%)
(3)若将ag该纯碱样品充分加热至无气体放出,冷却后称得剩余干燥固体的质量为bg(b<a).请写出该纯碱样品中Na2CO3的质量分数的表达式(要求写出计算过程).