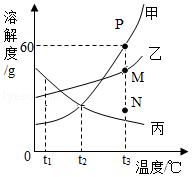
如图是甲、乙、丙三种固体物质的溶解度曲线。请回答下列问题:
(1)P点的含义是 。
(2)t2℃时,甲、乙、丙三种物质的溶解度大小关系为 。
(3)M、N分别是乙溶液t3℃时的两种状态,它们的溶质质量分数关系为M
N(填“=”、“<”或“=”)
(4)若将丙的饱和溶液从t3℃降温到t2℃时,一定会发生改变的是 (填序号);
A.溶解度
B.溶质的质量
C.溶质的质量分数
(5)现将t3℃时甲、乙的饱和溶液同时降温到t1℃,则析出晶体最多的是 (填“甲”、“乙”或“无法判断”)
海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等。综合利用海水制备金属镁的流程如下图所示: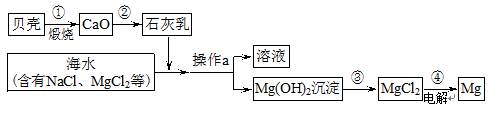
(1)贝壳主要成分的化学式是。 (2)操作a的名称是,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、。
(2)操作a的名称是,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、。
(3)工业冶炼镁常用电解MgCl2的方法,反应为:MgCl2 Mg+。
(4)写出第②、③两步反应的化学方程式:
②,③。
甲、乙两种固体的溶解度曲线如右图所示。
(1)℃时,甲和乙的溶解度相等;
(2)40℃时,若将40g乙(不含结晶水)放入160g水中充分溶解,所得溶液的溶质质量分数为,该溶液是
溶液(填“饱和”或“不饱和”);
(3)40℃时,将甲、乙两物质的饱和溶液各100g降温至20℃,析出晶体(均不含结晶水)的质量关系是:
m(甲)m(乙) (填“﹥”、“﹦”或“﹤”)。
目前部分农村的饮用水主要还是地下水。饮用遭到污染或硬度大的地下水不利于人体健康。政府积极建设自来水厂,让农民喝上清洁的水。
(1)检验某地下水是硬水还是软水,可用的物质是。
(2)测定地下水的酸碱度可用。(填标号)
A.紫色石蕊溶液B.无色酚酞溶液C.pH试纸
(3)自来水生产过程中,可用的方法除去水中不溶性杂质,同时还必须进行消毒。X是一种新型的自来水消毒剂,工业上制取X 的化学方程式为:
Cl2 + 2 NaClO2 ="=" 2 NaCl + 2 X,则X的化学式为。
实验小组的同学欲对一粗盐样品进行初步提纯。所用实验仪器或用品如下:
(1)A的名称是;
(2)提纯的步骤是:溶解、过滤、、计算产率;
(3)“过滤”操作的要点可概括为“一贴、二低、三靠”,其中“二低”的含义是
;
(4)实验小组通过正确的计算发现,所得实验结果对与该粗盐的实际含量对比,实验测得的结果比实际偏低,请分析可能的原因:
。
人体胃液中含有适量的盐酸,可以帮助消化,正常胃液的pH通常在0.9~1.5之间,胃酸过多或过少,都会引起胃部不适。
(1)治疗胃酸过多病症的药物中常含有的物质是(写一种即可);
(2)治疗胃酸过多的药物通常需嚼碎后服用,其原因是;
(3)有一些人因胃酸过少影响消化,他应该多吃的食物有(写一种即可)?