某样品由氧化铜和铜组成。取10.0g该样品于烧杯中,向其中加入92.0g稀硫酸,恰好完全反应后,过滤,所得滤液质量为100.0g。
(1)所取样品中铜的质量为 。
(2)从反应后所得的100.0g滤液中取出10.0g溶液,将其稀释为10%的溶液,需要加水多少克?
现将一定质量含氢氧化钠的碳酸钠固体中加入100g水充分溶解,向该溶液中逐滴加入溶质质量分数为10%的盐酸,生成气体的质量与加入盐酸的质量关系如图所示。
⑴当盐酸质量为150g时,溶液中溶质化学式为;
⑵求固体中碳酸钠的质量?(写出计算过程,保留一位小数)
⑶当充分反应后溶液中氯化钠的质量为g。
.为测定某地石灰石中碳酸钙的质量分数,兴趣小组同学取一定质量的石灰石于烧杯中,向烧杯中逐渐加入较浓的盐酸,反应过程测得剩余固体质量与加入盐酸的质量关系如图所示(石灰石中的杂质不与盐酸反应,也不溶与水)。请回答下列问题: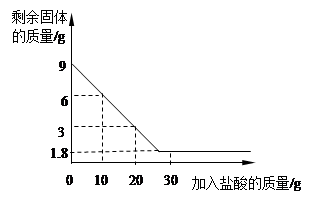
(1)石灰石中所含杂质的质量是 g。
(2)通过计算求所用盐酸的溶质质量分数。
(3)兴趣小组同学用测定产生的气体质量来求出石灰石中碳酸钙的质量分数,假如测量准确,通过计算得到的碳酸钙的质量分数比实际数值偏大,其原因可能是:。
(7分))课外活动时,同学们采用以下两种方法测定某氯化钠溶液的溶质质量分数。
(1)【化学方法】向一定量氯化钠溶液中加入足量硝酸银溶液,得到2.87g氯化银固体,则该氯化钠溶液中氯化钠的质量为多少?(根据化学方程式列式计算)
经多次实验测定,该溶液的溶质质量分数为10%。
(2)【物理方法】取一定量该溶液进行蒸发,测量实验数据如下:
| 蒸发皿的质量(g) |
25.0 |
| 蒸发皿+食盐溶液(g) |
45.0 |
| 蒸发皿+食盐晶体(g) |
27.4 |
| 数据处理 |
溶液的溶质质量分数为 |
若化学方法测定结果准确,则物理方法测定结果产生误差的原因是
A.蒸发时未用玻璃棒搅拌
B.所取氯化钠溶液质量较大
C.蒸发时出现少量晶体时就停止加热
D.实验后未将玻璃棒上的白色固体移入蒸发皿
(10分)市售珍珠粉的价格相差很大,但其外观、手感都没有明显差异,优质珍珠粉和廉价珍珠粉的成分有何不同呢?实验小组同学展开探究。
【查找资料】
①优质珍珠粉直接由贝科动物体内珍珠加工而成,含有一定量的氨基酸、碳酸钙等。
②廉价珍珠粉由“贝壳粉”加工而成,贝壳加工过程中会用到氢氧化钠,贝壳的主要成分是碳酸钙。
③珍珠粉中除碳酸钙外,其它成分均不能与盐酸反应生成二氧化碳。
④氨基酸大部分能溶解于水,遇到浓硝酸并加热会呈现黄色或黑色。
⑤碳酸钙与浓硝酸能发生反应,生成二氧化碳。
⑥氯化钙溶液呈中性。
【提出猜想】优质珍珠粉和廉价珍珠粉的区别可能在于:
①廉价珍珠粉含有;
②廉价珍珠粉不含氨基酸;
③碳酸钙含量不同。
【实验探究】
| 实 验 内 容 |
现 象 |
结 论 |
| (1)分别将少量优质珍珠粉和廉价珍珠粉放入试管中,加少量水,静置一段时间后,滴加。 |
廉价珍珠粉的上层清液变红,优质珍珠粉的溶液没有变色 |
猜想①成立 |
| (2)分别将少量优质珍珠粉和廉价珍珠粉放入试管中,加少量水,过滤, ,加热。 |
优质珍珠粉的溶液有黄色出现,局部变黑,廉价珍珠粉的溶液没有明显现象 |
猜想成立 |
(3)分别将一定质量的优质珍珠粉和廉价珍珠粉放入烧杯中,再逐滴加入14.6%的稀盐酸,边滴加边振荡,直至恰好完全反应。数据记录如下:
| 优质珍珠粉 |
廉价珍珠粉 |
|
| 珍珠粉的质量 |
100g |
100g |
| 加入盐酸的质量 |
460.0g |
500g |
| 烧杯中最终物质的总质量 |
520.0g |
558.2g |
①处理数据时,小明提出了如下思路:用加入盐酸的质量乘以盐酸的质量分数,求出反应的盐酸中的溶质质量,进而利用化学方程式(填写反应方程式)求出珍珠粉中碳酸钙的质量。
你认为小明的思路是否可行?(填“可行”或“不可行”)理由是。
②处理数据后,得出结论:廉价珍珠粉中碳酸钙的质量分数为%,含量高于优质珍珠粉。
某溶液中可能含有碳酸钠、氯化钾、硫酸钠、硫酸中的一种或几种,为测定其组成,进行如下实验:
取样20g,先后逐滴加入氯化钡溶液、稀硝酸,产生沉淀的质量与时间的关系如图所示.
(1)实验中,AB之间图象所对应的溶液中的溶质一定有 .
(2)BC段沉淀减少的原因是 (用化学方程式表示).
(3)由上述实验可知,原溶液中一定含有 ,可能有.
(4)求原溶液中硫酸钠的质量分数。