电子工业中常用覆铜板(以绝缘体为基材,表面覆以铜箔)为基础材料制作印刷电路板(如图所示)。印刷电路板广泛应用于电视机、计算机、手机等电子产品中。
某校初中科技小组的同学对于覆铜板制作印刷电路的原理很感兴趣,决定进行探究,请你随他们一起进行探究。
【查阅资料]
(1)覆铜板制作印刷电路的原理,是把预先设计好的电路在覆铜板上用蜡或不透水的物质覆盖,然后将覆铜板浸泡到FeCl 3溶液中,利用FeCl 3溶液将不需要的铜腐蚀掉,留下来的就是印刷电路。
(2)FeCl 3溶液呈酸性,在与铜单质反应后Fe 3+变为Fe 2+,反应后有Cu 2+产生。
【提出问题】FeCl 3溶液为什么能将铜腐蚀掉?
【猜想假设】
(1)小明同学从资料中获知FeCl 3溶液呈酸性,用石蕊试纸检验FeCl 3溶液,试纸变 色,他认为一定是溶液中的H +与Cu发生反应,将Cu腐蚀掉,但大家用 (填物质的化学式)不能与Cu反应置换出氢气的知识否定小明的观点。
(2)小文同学认为可能是FeCl 3溶液与铜发生了置换反应,Fe 3+将铜置换成可溶于水的Cu 2+,大家也否定他的观点,因为置换反应原理是 ,而不是一种离子置换另一种离子。
(3)根据查阅的信息,小丽同学认为这个腐蚀过程是一个新的反应,写出反应的化学方程式 。
【原理分析】根据信息和上述反应的化学方程式,得知铁元素由+3价下降为+2价的特点,从化合价的角度,小明同学又归纳出这个反应的另外两个特点:① ;② 。
【拓展研究】考虑到使用后的腐蚀液富含Cu 2+,具有很高的回收再利用价值,小组同学继续进行回收探究。在100mL反应后的废液中投入足量的锌粉,析出0.64gCu(若废液中仍有FeCl 3剩余,则锌粉先与FeCl 3反应,再与氯化铜反应),则说明原来配制的FeCl 3溶液浓度至少是 g/L(g/L是质量体积浓度的单位,表示的是在每升溶液中所含溶质的质量)。
【交流讨论】经思考,小丽同学推断FeCl 3溶液作为腐蚀液也可以与Fe发生反应。
请写出她的推断依据: 。

如图是某同学鉴别碳酸氢铵、硫酸铵、硝酸铵三种化肥的过程(反应条件未标出),请回答下列问题:
(1)步骤①中通过观察到现象,可以鉴别出碳酸氢铵.
(2)步骤②中所需试剂可以选用两种不同类别(按酸、碱、盐、氧化物进行分类)的物质,其化学式分别为、.
请写出硫酸铵分别与这两种试剂发生反应的化学方程式:、.
根据基础实验6"粗盐的初步提纯",填写相关实验内容:
(1)实验目的:学生可以初步学习除去粗盐中杂质的实验过程,…
(2)实验用品:粗盐、蒸馏水、玻璃棒、…
(3)实验过程:
实验步骤有:①计算产率 ②过滤 ③称量与溶解 ④蒸发
正确的操作顺序应是(填序号).
(4)问题讨论:
①实验过程中,多次用到玻璃棒.请你写出蒸发操作时玻璃棒的作用:.
②如果过滤后滤液仍浑浊,其原因可能是(写出一条).
如图是实验室制取气体的常用装置,请按要求填空:
(1)实验室用
装置制取氧气,反应的化学方程式为.若要收集较纯净的氧气,应选择的收集装置是.(填字母,下同).
(2)实验室制取二氧化碳,应选用的药品是(写名称),选择的发生装置是.
(3)
装置有多种用途.若在
中盛放,可以干燥二氧化碳;若用
收集
,证明氧气已经集满的方法是.
玻璃棒是化学实验室中常用的仪器,在许多化学实验中都用到它.
(1)在过滤操作中,玻璃棒的作用是.
(2)在蒸发操作中,使用玻璃棒的目的是.
(3)在溶解氯化钠时,用玻璃棒不断搅拌可以.
(4)在稀释浓硫酸时,用玻璃棒不断搅拌是为了.
图是某化工厂生产烧碱的工业流程图.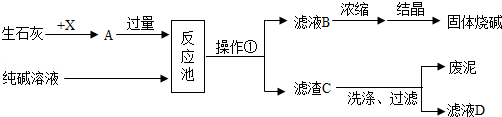
请根据以上信息回答下列问题:
(1)请写出
物质在实验室中的一种用途.
(2)反应池中发生反应的化学方程式为.
(3)操作①的名称是,结晶得到的固体烧碱中可能含有少量的(写化学式).
(4)滤液
可加入反应池循环再利用,目的是降低生产成本和防止.