工业上利用某废渣【含FeSO4、Fe2(SO4)3及少量CaO和MgO】制备高档颜料铁红(主要成分为Fe2O3)和回收(NH4)2SO4.具体生产流程如下:

【背景信息】
a.氧化还原反应中,会有元素化合价发生变化。
b.3Fe2(SO4)3+12NH3•H2O=(NH4)2Fe6(SO4)4(OH)12↓(铵黄铁矾晶体)+5(NH4)2SO4
(1)步骤③中操作Y的名称是 。
(2)加入物质X溶解废渣,X应选用 (填序号)。
A.盐酸 B.硫酸 C.氨水 D.氢氧化钠
步骤①酸浸时,生成盐的化学方程式为 (任写一个)。
(3)步骤②通入氧气氧化的目的是 ;工业上对该操作控制在4小时左右为宜,根据如图有关数据分析,影响Fe2+氧化率的变化规律: 。

2011年3月12日,贵州省六盘水市盘县松河乡已公告关闭的金银煤矿发生重大瓦斯爆炸事故,共造成19人死亡、15人受伤,人员伤亡惨重,经济损失巨大.
(1)请从燃烧的条件着手分析这次爆炸发生的原因.
(2)根据你所学的知识,简要的说说如何预防矿井内瓦斯爆炸.(答出2条即可)
小宇同学完成了教科书中“给液体加热”的实验后,想试着做对固体加热的实验:他取了一只试管,加入蔗糖固体后放在酒精灯上加热,但过了一会儿,却发现试管炸裂。请你帮他分析一下,造成试管炸裂的原因。(只要求写出一种原因)
已知A、B分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示向A中加入B时,溶液pH变化曲线.请写出你从曲线图中收获的信息: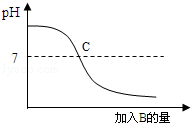
(1)A是 ;
(2)B是 ;
(3)C点表示 .
发生火灾时,一定要将附近的液化石油气罐尽快搬离火场,因为高温时,液化石油气瞬间体积膨胀250~300倍,罐内压力骤然增大致使罐体破裂而发生第一次爆炸;当泄漏出的石油气在空气中的浓度降至3%~11%时,遇明火将发生第二次爆炸.
(1)用微粒的观点解释第一次爆炸发生的原因.
(2)分析第二次爆炸为什么会发生?
请用所学化学知识解释下列原理。
(1)6000L氧气在加压的情况下可以装入40L的钢瓶中。
(2)从微观角度解释CO2和CO元素组成相同,但二者性质却差异很大。
(3)用化学方程式表示工业上用焦炭与铁矿石(主要成分Fe2O3)反应炼铁。
(4)做木炭在氧气里燃烧实验时,红热的木炭为什么要由瓶口向下缓慢插入?